引言:一周一见的CDE药品审评周报来了! 恒瑞医药管线又添新、必贝特银屑病治疗药物首次报临床、新型BTK抑制剂首次报临床!详情见下(文中统计结果不包括补充申请&进口再注册)。
创新药承办情况
2022年2月14-20日CDE共承办27个创新药受理号,其中包括了化药受理号15个,生物制品受理号12个,无中药受理号。此次的27个1类新药受理号均为临床试验申请,无上市注册申请。
化药创新药
此次申报的化药分别为HS-10384片、R01散、TT-01488片、EVER001胶囊、SR750片、SYHX2005、XTR006注射液、BEBT-305片、注射用聚乙二醇伊立替康。
HS-10384片为首次申报临床,来自豪森子公司上海瀚森生物,暂未披露靶点及适应症。
TT-01488片也为首次申报临床,根据药捷安康官网披露信息,TT-01488片是药捷安康在研新型非共价的可逆BTK抑制剂。该产品有望克服由共价BTK抑制剂引发的获得性耐药,应用于多种复发性或难治性血液恶性肿瘤。
BEBT-305此次为首次申报临床,是一种Chaperone蛋白抑制剂。根据必贝特官网披露信息,BEBT-305可通过下调或降解参与自身免疫和炎症相关的多种细胞因子,抑制T-细胞参与的自身免疫和炎症反应。目前,PDE4抑制剂阿普斯特是FDA批准用于治疗银屑病的唯一口服靶向治疗药物。中国大约有650万银屑病患者,目前尚无有效口服药物治疗。必贝特国外合作伙伴正在欧洲开展BEBT-305治疗银屑病Ib临床试验。
SYHX2005为首次申报临床,来自石药集团欧意药业,暂未披露靶点及适应症。
生物制品创新药
此次申报的生物制品分别为:人脐带间充质干细胞注射液、SHR-2010 注射液、Olvi-Vec注射液、DB-1202注射液、PM8002注射液、人源TH-SC01细胞注射液、CPD-002注射液、注射用8MW2311、异体内皮祖细胞(EPCs)注射液、注射用重组人源化抗HER2单抗-AS269偶联物(ARX788)。
SHR-2010 注射液来自恒瑞医药,为首次申报临床,暂未披露靶点及适应症。
PM8002注射液最早被CDE承办的临床试验申请可追溯到2020年8月。根据普米斯生物官网信息,PM8002为一款靶向PD-1/VEGF的生物药,适应症为三阴性乳腺癌。
注射用 8MW2311来自迈威生物,为首次申报临床。 注射用 8MW2311是一种聚乙二醇偶联人白介素-2 免疫激动剂,用于治疗晚期恶性肿瘤。注射入体内后,可刺激下游转录因子 STAT5 磷酸化,有效激发杀伤性 T 淋巴细胞 CD8+T 细胞的增殖,从而发挥药效。临床前研究结果显示,8MW2311 在肿瘤组织中富集并具有偏好地激活 CD8+T 细胞的药理作用,在多种肿瘤模型中显示出持续有效的抑瘤作用,并且与免疫检查点药物(如抗 PD-1 抗体)联用能表现出显著性增强的协同抑瘤效果。
创新药承办情况
改良型新药承办情况
2022年2月14-20日CDE共承办5个改良型新药受理号。包括化药受理号1个,生物制品受理号1个,中药受理号3个。
唯一承办的化药改良型新药为南京海融医药科技的注射用HR1801。根据海融医药官网披露信息,HR1801的适应症为术后镇痛。
3个中药受理号均来自江苏康缘药业,分别为苁蓉总苷胶囊、大株红景天胶囊以及金振口服液。
改良型新药承办情况
一致性评价承办情况
2022年2月07-13日CDE共承办24个一致性评价受理号,详情见下表。
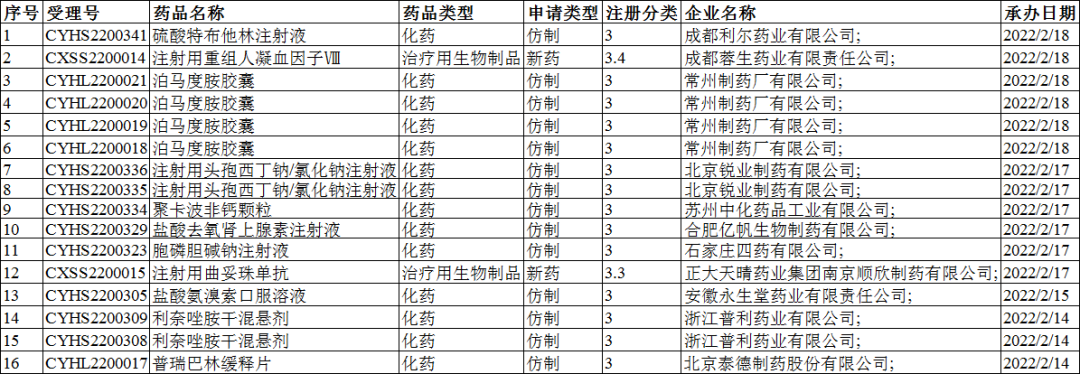
注册分类:3类
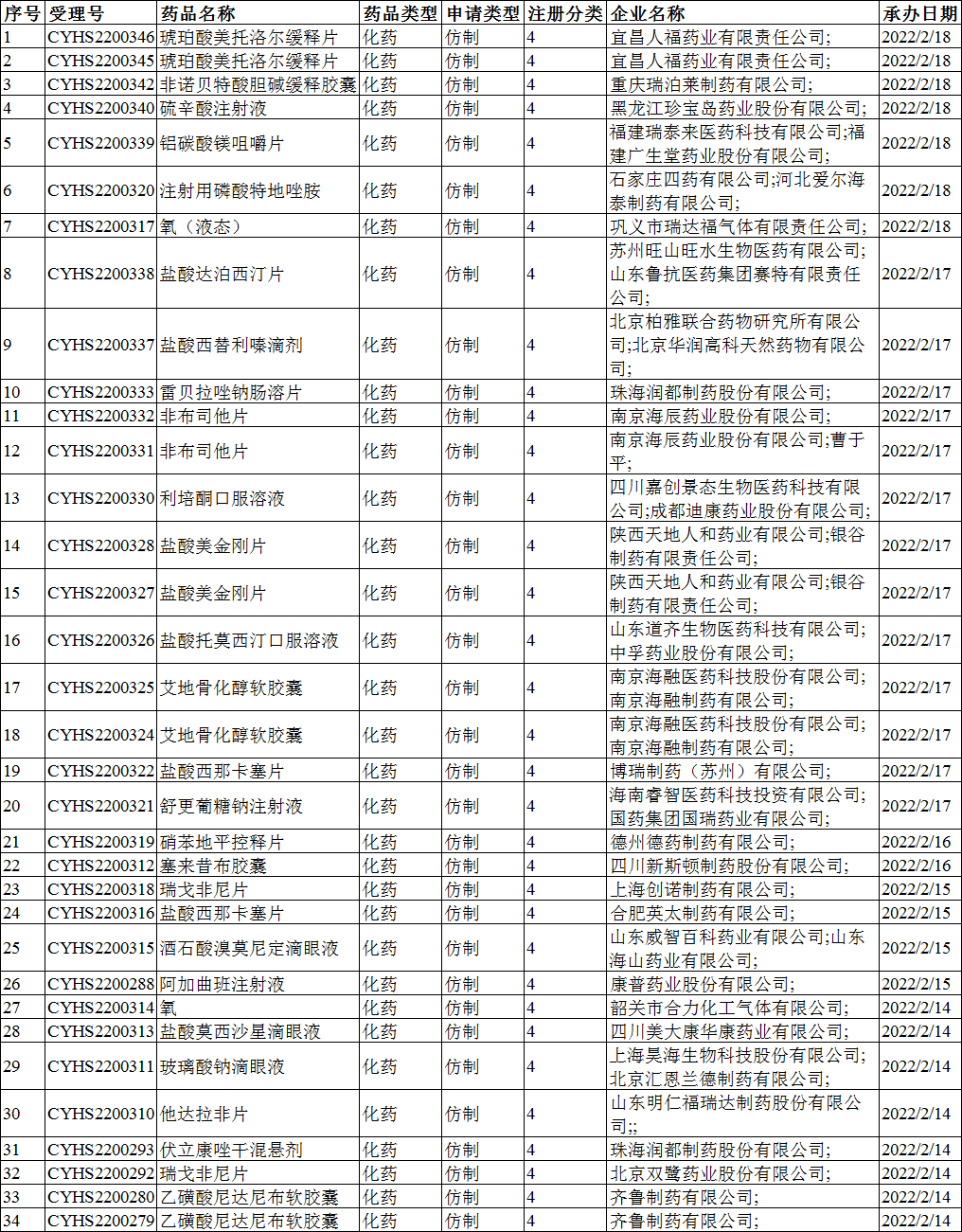
注册分类:4类
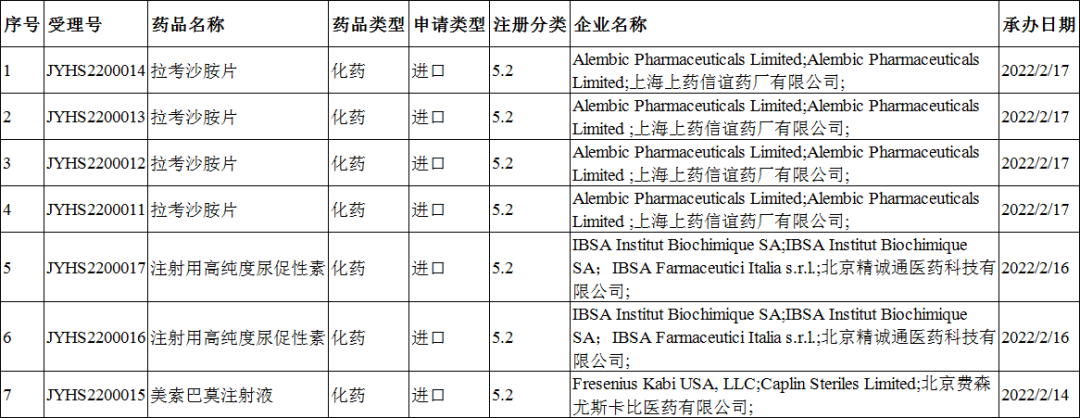
注册分类:5类













收藏
登录后参与评论