以下为药融圈旗下
药融云数据(网址:www.pharnexcloud.com)针对
2021年中国药企License out海外药企的大盘点(排版不分先后),
新药海外授权已经成为常态化。当然国内企业之间交易也火热进行中;合作开发是生物医药转型升级的必经之路。
01、高诚生物
2021年12月20日,FibroGen, Inc. (Nasdaq: FGEN),与一家在免疫调节和单细胞科学领域具有丰富经验的跨国临床阶段生物制药公司高诚生物,宣布达成一项拓展合作,FibroGen对高诚生物的抗CCR8单克隆抗体项目(HFB1011)行使独家许可选择权。
根据协议条款,FibroGen将向高诚生物支付3500万美元首付款,之后将支付可能的临床、注册和商业化里程碑款。高诚生物还将有资格获得基于净销售额的特许权使用费。
FibroGen将获得在全球范围内开发CCR8项目所有产品的独家授权。候选抗体预计将于2023年进入临床试验阶段。(CCR8属于GPCR类受体,在多种不同类型肿瘤中浸润的介导免疫抑制的调节性T细胞(Tregs)有普遍和高特异表达。其配体可刺激CCR8,导致肿瘤微环境中的Tregs增殖和免疫抑制。靶向CCR8的抗体可通过抗体依赖的细胞毒(ADCC),选择性地杀伤和清除肿瘤微环境中高度免疫抑制的Tregs,从而促进抗肿瘤免疫。)
此前在,2021年6月15日FibroGen与高诚生物建立战略合作。FibroGen获得Galectin-9项目所有抗体的独家许可权,有权在全球范围内独家开发、生产和商业化这些抗体。据协议,高诚生物获得2500万美元的首付款和未来至高11亿美元的里程碑付款以及基于产品全球净销售额的特许权使用费。
02、百济神州
百济神州将TIGIT抗体ociperlimab的主要海外权益以29亿美元价格授权给诺华。首付款为3亿美元,具体合作信息如下:
03、锐格医药
锐格医药(Regor Therapeutics )与礼来制药达成的合作是针对GLP-1R靶点RGT-075的专利许可,交易总金额达15.5亿美元(预付款5000万美元,里程碑15亿美元)。这项高额交易针对的是尚在临床前阶段的备选专利。此外,锐格医药的GLP-1R的小分子化合物RGT-075在临床阶段;临床前阶段肿瘤候选新药RGT-419B、RGT-197等等。
CARD(Computer Accelerated Rational Discovery)
04、荣昌生物
国内ADC龙头企业荣昌生物(09995.HK)与国际知名生物制药公司西雅图基因(Seagen Inc. 纳斯达克:SGEN)达成一项全球独家许可协议:
针对荣昌生物的ADC新药维迪西妥单抗(RC48,商品名:爱地希),Seagen 将付出 2 亿美元首付款+最高 24 亿美元的里程碑付款,以获得该药物全球部分地区的开发和商业化权益。这笔交易刷新了由百济和诺华创造的国内单品海外授权交易金额的最高纪录。
根据协议内容,维迪西妥单抗在大中华区、亚洲所有其他国家(日本、新加坡除外)的开发和商业化将继续由荣昌负责,而全球其他地区的权益则归Seagen所有。但协议规定:Seagen 还需要向荣昌生物支付根据维迪西妥单抗在 Seagen 地区销售的金额计算的特许权使用费,以及金额为产品累计销售净额的高个位数至百分之十几的比例提成。
05、诺诚健华
2021年7月13日,诺诚健华公告称,公司与
渤健就BTK抑制剂
奥布替尼(orelabrutinib)达成许可及合作协议,诺诚健华将获得1.25亿美元首付款,以及至多8.125亿美元的里程碑付款。
奥布替尼治疗领域涉及肿瘤、血液系统、免疫调节,其针对慢性淋巴细胞白血病、套细胞淋巴瘤的适应症于2020年12月获得中国国家药品监督管理局批准。奥布替尼成为继伊布替尼、泽布替尼后,国内第三款上市、国产第二款BTK抑制剂。
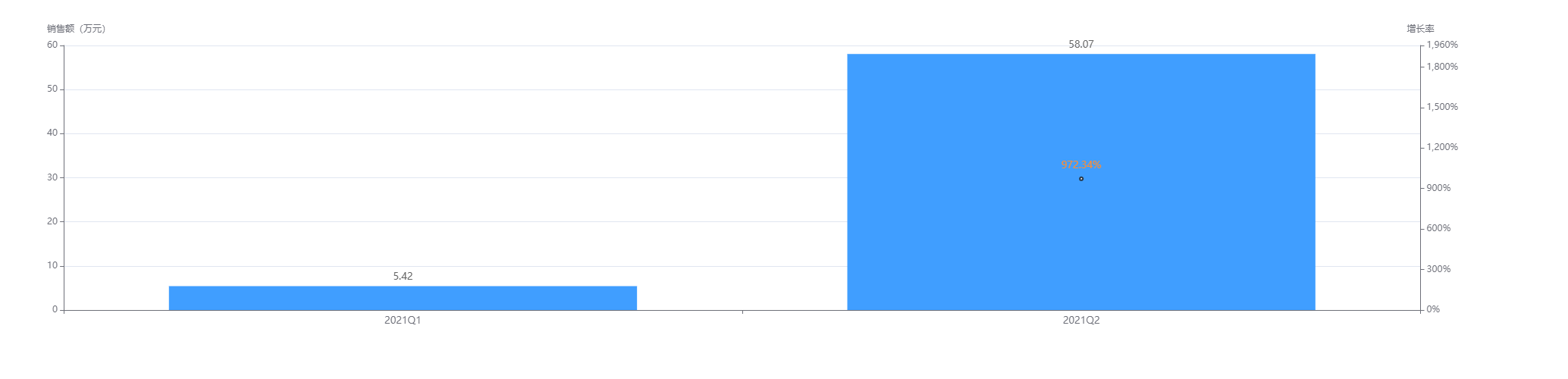
据药融云销售数据库显示,诺诚健华的奥布替尼2021年1月正式上市,2021年Q1季度的销售额为5.42万元,Q2季度开始走红,销售额直达58.07万元,同比增长972%,2021全年销售额有希望冲击200万。
截图来源:药融云全国医院销售数据库
06、艾力斯
2021年7月1日,艾力斯公告称,公司与ArriVent公司达成海外独家授权合作协议,ArriVent公司将获得伏美替尼除中国(中国大陆、香港、澳门和台湾地区)以外全球其他地区的独家开发及商业化许可权。艾力斯将获得4000万美元首付款及ArriVent公司部分股权,可高达7.65亿美元的里程碑付款,以及可高达两位数的销售提成。
伏美替尼属于第三代表皮生长因子受体-酪氨酸激酶抑制剂(EGFR-TKI),于 2021 年 3 月在中国获批用于 EGFR T790M 突变阳性局部晚期或转移性非小细胞肺癌 (NSCLC) 适应症。2021年第二季度的销售额为32.6万元。该公司专注于靶向癌症疗法的研发、制造和商业化——正在积极研究伏美替尼在中国其他 EGFR 突变 NSCLC 患者群体中的转移和辅助临床环境的潜力。(
新锐|Arrivet完成1.5亿美元A轮融资,超8亿美元与艾力斯达成合作)
07、华东医药
2021年9月,华东医药全资子公司杭州中美华东制药与韩国Daewon达成战略合作。Daewon获得华东医药小分子GLP-1受体激动剂TTP273在韩国的独家开发、生产及商业化权利,华东医药将会继续负责TTP273在中国以及亚太其它地区的研发、生产和商业化。根据协议,华东医药将获得150万美元首付款,高达3750万美元的里程碑付款,以及约定比例的净销售额分成。
TTP273是一款口服小分子非肽GLP-1受体激动剂,拟开发用于治疗2型糖尿病,目前正在开展临床2期试验。
08、普瑞金生物
2021年5月9日,普瑞金生物与印度瑞迪博士达成授权合作,瑞迪博士获得靶向BCMA的嵌合抗原受体T细胞注射液在印度地区的独家权益。普瑞金将获得500万美元的首付款和里程碑付款,以及后续针对其他适应症的不超过750万美元的里程碑付款,并享有不超过1.5亿美元的商业化销售分成。
09、济民可信
2021年11月30日,济民可信子公司上海济煜医药科技有限公司(以下简称“上海济煜”)与沪亚生物国际(以下简称“沪亚”)(HUYABIO INTERNATIONAL)达成一项独家许可协议,上海济煜将具有自主知识产权的KRAS抑制剂JMKX1899在大中华区以外的开发、生产及商业化权利独家许可给沪亚,JMKX1899在大中华区域的相关权益仍归济民可信所有。
JMKX1899是上海济煜小分子创新中心自主研发的KRAS抑制剂,临床前研究数据显示,与同靶点产品相比,JMKX1899具有较强的脑通透性,且没有心脏毒性和药物-药物相互作用风险。上海济煜将同步推进JMKX1899在中国和美国的临床。(
HUYA崭露头角:从中国淘金的海外的Biotech)
10、上海医药
2021年10月28日,上海医药以不超过2.925亿美元(除销售提成外)的交易金额将具有自主知识产权的SPH6162的海外权益许可给HUYABIO。SPH6162为上海医药中央研究院自主研发的抗肿瘤小分子抑制剂。通过抑制激酶活性,抑制肿瘤细胞对药物的损伤修复,从而达到对肿瘤细胞杀伤。
SPH6162目前处于临床前开发阶段,已提交两款化合物的国际专利申请。SPH6162为全球同靶点研发快速跟进产品,借助海外合作伙伴的资源和研发力量,有望加快该产品在国内外的同步开发速度。药融云数据(www.pharnexcloud.com)显示,本品是一款Wee1新药。
11、绿叶制药
2021年2月18日,绿叶制药集团宣布,旗下子公司绿叶制药(瑞士)与Towa Pharmaceutical(东和药品)达成协议,授予后者在日本市场开发及商业化利斯的明多日透皮贴剂的独家权利。
3月16日,绿叶制药集团再次宣布已与Italfarmaco集团达成协议,授予后者在德国、意大利、葡萄牙和希腊四个欧洲国家商业化其利斯的明多日透皮贴剂的独家权利,Italfarmaco集团同时还拥有在智利和越南商业化该产品的优先权利。
12、北京泰德
2021年2月24日,北京泰德制药与美国Graviton签订海外授权合作协议,在大中华以外地区共同开发及商业化其自主研发的治疗纤维化创新药TD101(Rock2抑制剂),中国生物制药将获得Graviton支付的首付款、TDI01开发阶段的里程碑付款,以及TDI01上市后专利期内按销售收入比例支付的许可费、销售里程碑付款,合计最高可达到5.175亿美元。北京泰德为港股中国生物制药子公司。
13、君实生物
2021年2月1日,君实生物公告与
Coherus就PD-1单抗
特瑞普利单抗注射液(toripalimab)在美国和加拿大的开发和商业化达成合作。君实生物将获得总额最高达11.1亿美元的首付款、可选项目执行费和里程碑付款,同时授予Coherus其
JS006(抗TIGIT单抗)和
JS018-1(新一代改良IL-2细胞因子药物)的选择权,以及君实生物2个早期阶段检查点抑制剂抗体药物的优先谈判权。
据药融云销售数据库显示,君实生物的特瑞普利单抗注射液2019年在全国医院的销售额为0.86亿元;2020年1.49亿元,同比增长72.69%;2021年前两个季度的销售额已有1.14亿元,全年销售额将突破2亿大关,有希望冲击3亿。
截图来源:药融云全国医院销售数据库
14、百济神州
北京时间2021年1月12日,百济神州宣布与诺华达成一项合作与授权协议,在多个国家包括美国、加拿大、墨西哥、欧盟成员国、英国、挪威、瑞士、冰岛、列支敦士登、俄罗斯和日本开发、生产和商业化抗PD-1抗体百泽安®(替雷利珠单抗)。双方将在上述国家对百泽安®进行共同开发,其中诺华将在过渡期后负责注册申请,并在获得批准后开展商业化活动。此外,双方均可在全球范围内开展临床试验以评估百泽安®联合其他抗肿瘤疗法的潜在用药组合;百济神州可在北美地区共同进行产品销售,其中部分运营资金将由诺华提供。根据协议,百济神州将获得6.5亿美元的预付款,并有资格在达到注册里程碑事件后获得至多13亿美元的付款、在达到销售里程碑事件后获得2.5亿美元的付款,另有资格获得百泽安®在授权地区未来销售的特许使用费。
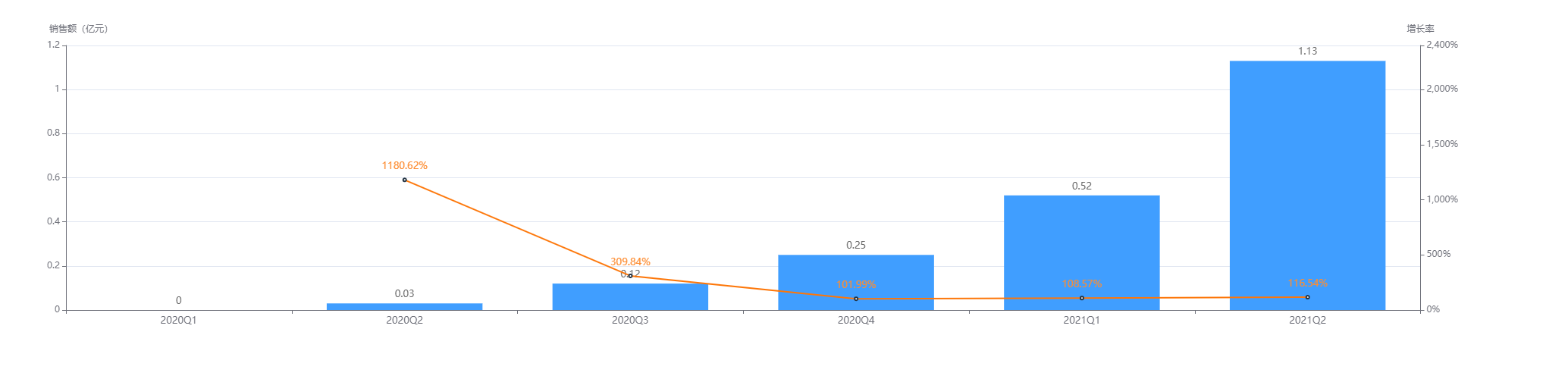
据药融云全国医院销售数据库显示,百济神州的替雷利珠单抗开卖以来,每个季度销售额呈阶梯式增长,一年比一年高一倍,并于2021年第2季度达到最高值1.13亿元,预计还会持续增长下去。
截图来源:药融云全国医院销售数据库
15、百奥泰
2021年4月8日,渤健与百奥泰生物联合宣布,双方签署了关于开发、生产和商业化BAT1806(托珠单抗生物类似药)的授权协议。根据协议,渤健将获得BAT1806在除中国(中国大陆、香港、澳门和台湾地区)以外全球所有国家的注册、生产和商业化相关的独占权利。BAT1806是一款靶向白介素-6受体(IL-6R)的重组人源化单克隆抗体,是百奥泰生物参照雅美罗(托珠单抗)开发的生物类似药。渤健向百奥泰生物支付首付款3000万美元。目前针对类风湿性关节炎的适应症在中国已提交上市申请。
2021年8月27日,百奥泰和
Hikma宣布,双方就
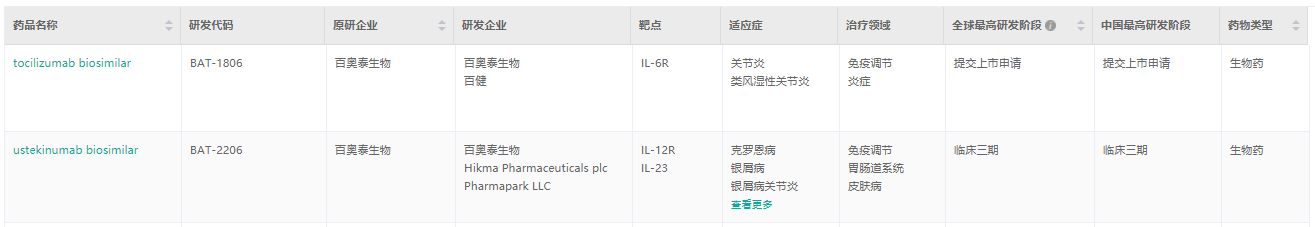
乌司奴单抗生物类似药BAT2206签署了在美国市场的独家商业化及授权协议。Hikma将获得BAT2206在美国市场的独家商业化权益,以及在欧洲市场(不包括独联体国家)关于该候选药的优先谈判权。百奥泰将负责BAT2206的开发、生产和供应。根据协议条款,百奥泰获得2000万美元的首付款,以及最高达1.3亿美元的开发和商业化里程碑付款。(
高质量biosimilar授权大药厂;百奥泰深耕的新药还有哪些布局?)
截图来源:药融云全球药物研发数据库
16、科伦博泰
2021年3月25日,科伦博泰与Ellipses Pharma达成区域授权合作协议。根据协议,科伦博泰将其小分子肿瘤靶向RET激酶抑制剂项目(A400项目)的欧美等区域权利有偿独家授权给Ellipses Pharma公司,科伦博泰则保留该项目在大中华区及韩国、新加坡、马来西亚等部分亚太地区的权利。双方将在各自区域内进行开发、商业化等活动,并利用各自区域内数据支持项目全球研发。药融圈预计,科伦药业将分拆新药部分(科伦博泰)上市。
17、科济药业
科济药业2021年上半年度业绩报告披露,子公司CAFA therapeutics与韩国HK inno.N公司已就科济药业开发的两款细胞疗法产品的开发和商业化达成许可及协议。分别为:CT032,一款靶向CD19的自体CAR-T候选产品;CT053,一款靶向BCMA的自体CAR-T产品。根据协议条款,科济药业将获得总计达5000万美元的预付款和额外的里程碑付款,并有资格获得基于合作约定产品在韩国未来净销售额的特许权使用费。
18、丽珠医药
2021年11月15日,丽珠集团子公司丽珠单抗与Bright Peak公司达成研究合作和授权许可协议。根据协议,Bright Peak 公司获得丽珠单抗公司的抗PD-1单抗LZM009有偿非独家许可,用于开发新型PD-1靶向免疫细胞因子(PD-1 ICs),并获得授权在除大中华区以外的区域用LZM009开发及商业化PD-1 ICs药物。
19、信达生物
2021年1月14日,信达生物将其贝伐珠单抗生物类似药(IBI301)在美国和加拿大的商业化权益授权给Coherus,并将授予Coherus在美国和加拿大开发和商业化信达生物的利妥昔单抗生物类似药(IBI301)的非排他性优先选择权。1月19日,信达生物与Etana公司签订合作协议,授予Etana贝伐珠单抗生物类似药在印度尼西亚的独家许可。
2021年1月29日,信达生物发布内幕消息公告,其PD-1单抗达伯舒(信迪利单抗注射液)2020年全年销售收入超过22亿元人民币,第四季度超过7亿元人民币。作为首个进入国家医保目录的PD-1抑制剂,达伯舒(信迪利单抗注射液)2020年收入实现同比大幅增长。(
PD-1全年大卖22亿元,信达生物产品管线长啥样?)
20、石药集团
2021年8月18日,石药集团附属公司NovaRock与Flame Biosciences订立策略合作及许可协议。根据协议,NovaRock将获得750万美元的首付款、至多1.725亿美元的开发里程碑款项、至多4.6亿美元的销售里程碑款项,以及净销售额若干百分比的提成。
NovaRock将授予Flame在大中华以外地区开发、制造及商业化NBL-015的独家权利。此外,NovaRock将利用其NovaTE 双特异性抗体技术平台与Flame合作开发两款新型双特异性抗体,并授予在大中华以外地区开发、制造及商业化该两款新型双特异性抗体的独家权利。NBL-015是一种全人源抗Claudin 18.2单克隆抗体。
21、索元生物
2021年4月14日,索元生物与Rumpus Therapeutics签订了开发DB102(enzastaurin)用于治疗血管性埃勒斯-当洛综合征(vEDS)等罕见遗传病的全球授权协议。根据协议,Aytu BioPharma将负责DB102针对这一罕见病的临床开发及商业化,并将支付索元生物总计1亿美元的里程碑付款及销售提成。
参考:
NMPA/CDE;
药融云数据 www.pharnexcloud.com;
FDA/EMA/PMDA;相关公司公开披露;
https://hifibio.com/;
中国
创新药交易的两面,引入渐现前沿靶点、输出成为出海路径;
https://www.regor.com/;
锐格与礼来,https://investor.lilly.com/news-releases/news-release-details/lilly-and-regor-therapeutics-group-enter-strategic-collaboration;
http://www.remegen.cn/;
《Success Factors in Product Licensing in the Pharmaceuticals Industry》;
百济神州,https://mp.weixin.qq.com/s/zqUHoOQVhAFlxAPo2SiCZg;
https://cn.innocarepharma.com;
https://www.allist.com.cn/;
https://www.luye.cn/lvye/;
http://www.tidepharm.com;
https://www.junshipharma.com/;
https://www.bio-thera.com/;
Ma H , Huang W , Wang X , et al. Structural insights into the activation of GLP-1R by a small molecule agonist[J]. Cell Research.;
Trends in oncology drug innovation in China,https://www.nature.com/nrd/;
Chinese biopharma starts feeding the global pipeline,https://www.nature.com/articles/nrd.2017.94;
中国新药授权合作掀高潮,商业化成license-in谈判关键因素 ,https://www.iyiou.com/p/131096.html ;
https://huyabio.com/pipeline/;
等等。
<END>










































收藏
登录后参与评论