01
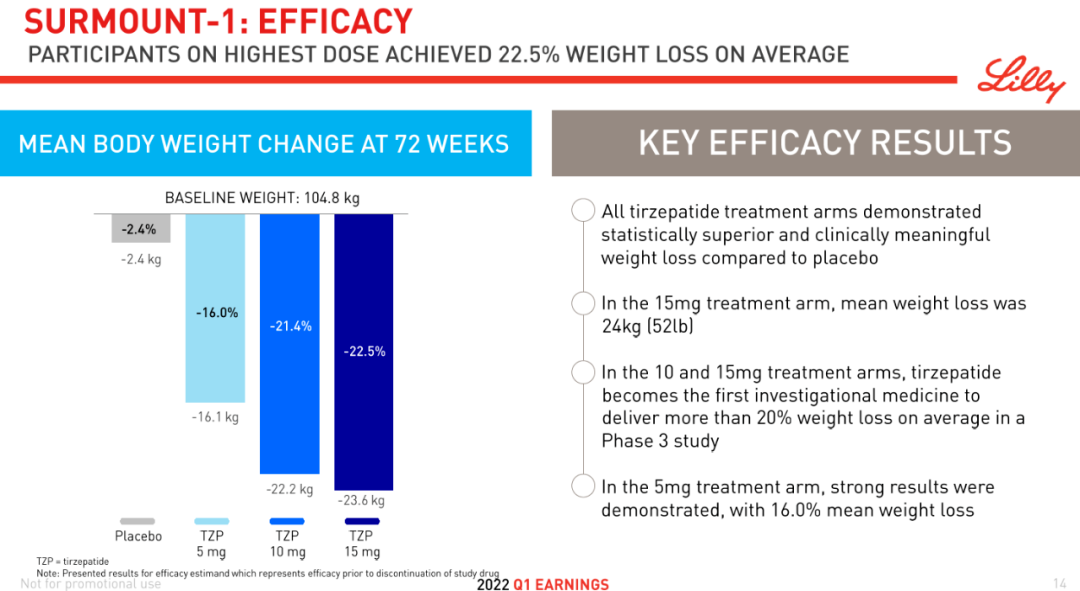
2022年4月28日,礼来制药公布潜在重磅新药GLP1/GIP双受体激动剂Tirzepatide(皮下注射的周制剂)的一项为期72周的安慰剂对照研究SURMOUNT-1研究的关键数据。该研究主要目的是评估Tirzepatide对肥胖或至少有一种合并症的超重的非糖尿病成年患者的疗效和安全性,是Tirzepatide在肥胖或超重成年患者中开展的首个全球III期注册研究。
SURMOUNT-1研究共纳入 2,539 名受试者,结果显示:Tirzepatide(5mg,10 mg,15mg)组受试者治疗第72周体重降低显著优于安慰剂,最高体重降幅可达22.5%(24 公斤),Tirzepatide治疗组体重降幅超过 5% 的受试者百分比更高。该研究在72周亦实现了所有关键次要终点。(需关注患者的基线)
02
2021年10月26日,礼来制药宣布已经向美国FDA提交了Tirzepatide的2型糖尿病适应症新药上市申请(NDA),同时附上了一张优先审评券,以加快Tirzepatide上市。礼来预计从提交上市申请到获批需要历时约8个月,也就是最快在今年的6月底可能迎来Tirzepatide获批。此前有分析机构预测,Tirzepatide上市后到2026年的销售峰值达50亿美元。
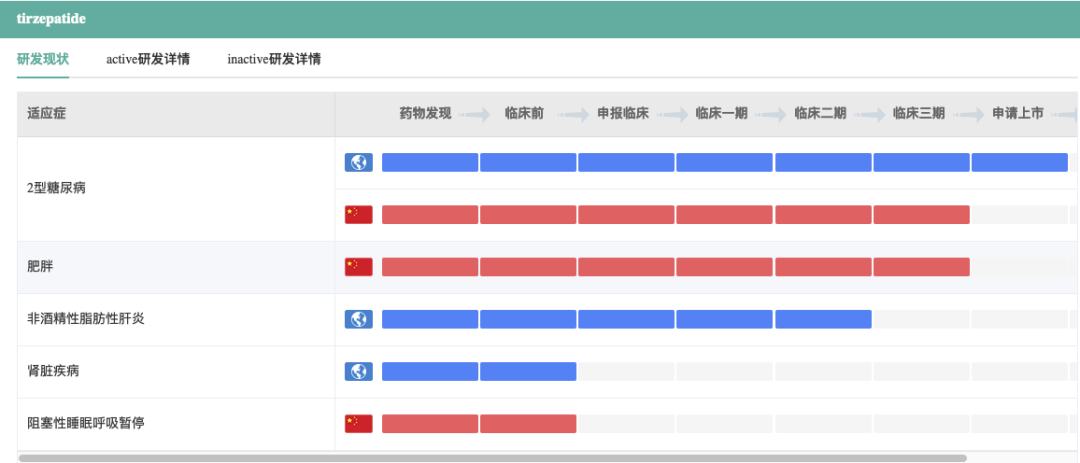
Tirzepatide适应症研发现状
▲药融云数据中本品全球进展
03
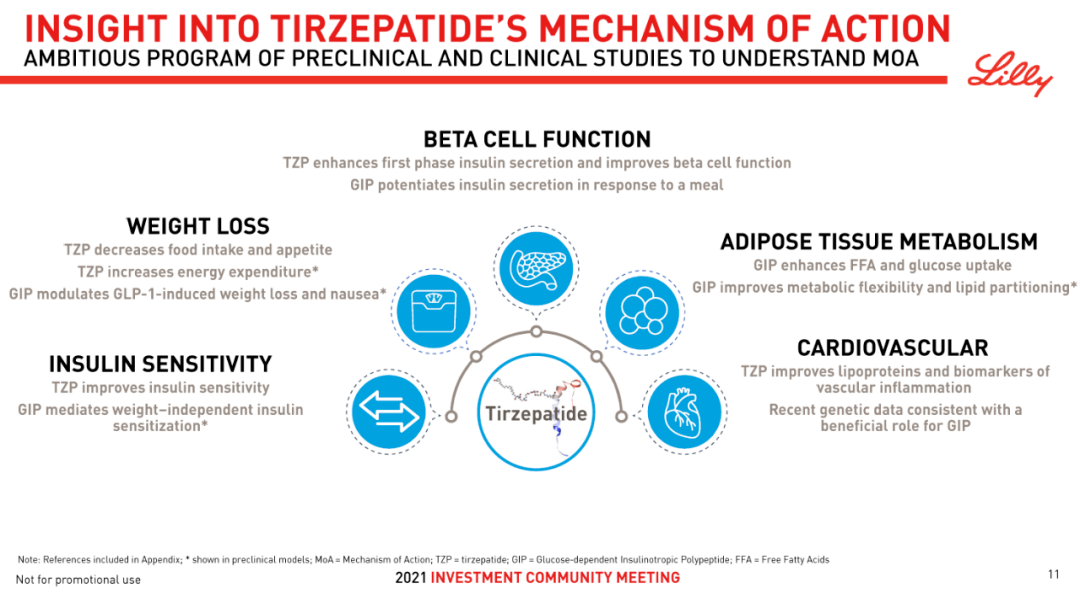
Tirzepatide作为一种每周一次的葡萄糖依赖性促胰岛素多肽(GIP)和胰高血糖素样肽-1(GLP-1)的双受体激动剂,一个分子实现两种肠促胰素的作用整合,相关专利WO-2016111971。GIP是一种肠促胰素,能够补充GLP-1受体激动剂的作用。在临床前模型中,已证明GIP可减少摄食量并增加能量消耗,从而减轻体重,当联合GLP-1受体激动剂时,可能对代谢紊乱如体重、血糖和血脂产生更大的影响。对于降糖或减重不同的适应症,礼来此前表示将实行双品牌策略(类似于诺和诺德的Wegovy和Ozempic)。
此外,Tirzepatide对于非酒精性脂肪性肝炎(NASH)和射血分数保留的心衰(HFpEF)的治疗方案也在临床研究过程中。在阻塞性睡眠呼吸暂停 (OSA)(中国临床试验也获得许可) 和肥胖发病率/死亡率方面的应用亦进行研究。 Tirzepatide临床试验总投入将达到28亿美元,慢性疾病的天花板之一。
▲药融云数据中本品中国临床试验情况
04
国际糖尿病联盟(International Diabetes Federation,IDF)2021年全球糖尿病地图显示,2021年全球成年糖尿病患者数量达到5.37亿例,全球约1/10的成年人受到影响。与2019年相比,糖尿病患者增加了7400万例,增幅达16%。预计到2025年,糖尿病患病率将进一步上升至12.2%,患病人数将增加到7.83亿例。2021年约有670万人死于糖尿病或糖尿病并发症,占到了全因死亡人数的12.2%。糖尿病在全球范围内造成的医疗卫生支出将近1万亿美元,占总医疗卫生支出的9%。
中国是成人糖尿病患者最多的国家,过去的10余年间(2011至2021年),我国的糖尿病患者由9 000万例增加至1.4亿例,增幅达56%,其中约7 283万例患者尚未被确诊,比例高达51.7%。另外,约有1.7亿成人伴有糖耐量受损,约2 700万成人伴有空腹血糖受损,这些人群都是糖尿病人群的“后备军”。预测到2045年,中国糖尿病患者数量将达到1.744亿例。
05
肥胖症是指机体脂肪总含量过多和/或局部含量增多及分布异常,是由遗传和环境等多种因素共同作用而导致的慢性代谢性疾病。肥胖主要包括3个特征:脂肪细胞的数量增多、体脂分布的失调以及局部脂肪沉积。通过减重预防和治疗肥胖相关性并发症改善患者的健康状况。肥胖症患者体重减轻5%~15%或更多可以显著改善高血压、血脂异常、非酒精性脂肪肝、2型糖尿病患者的血糖控制,降低2型糖尿病和心血管并发症的发生率。
《中国居民营养与慢性病状况报告(2020年)》数据显示:我国成年居民超重肥胖超过50%;具体而言成年人(≥18岁)中超重和肥胖比率分别为34.3%和16.4%;18岁及以上居民男性和女性的平均体重分别为69.6千克和59千克,与2015年发布结果相比分别增加3.4千克和1.7千克。城乡各年龄组居民超重肥胖率继续上升。
06
刚刚过去的5月11日,是世界防治肥胖日。未来这类慢性疾病将高发,药融云数据,https://www.pharnexcloud.com/?zmt-mhwz显示:目前国内布局GLP-1受体激动剂类新药(含多靶点)的企业有:信达生物、恒瑞医药、豪森药业、先为达、华东医药及道尔生物、锐格医药、众生睿创、奥达生物、硕迪生物、北京质肽生物、甘李药业、安源生物、博瑞生物、银诺医药、仁会、鸿运华宁、华健未来、昂博制药、赛诺生物、晟斯生物、诚益生物、派格生物等。
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场
参考:
NMPA/CDE;
药融云数据,https://www.pharnexcloud.com/?zmt-mhwz;
FDA/EMA;
相关公司公开披露;
https://investor.lilly.com/news-releases;
https://diabetesatlas.org/data/en/;
Solid First-Quarter Financial Results Reflect Lilly's Continued Momentum into 2022. ;https://investor.lilly.com/news-releases/news-release-details/solid-first-quarter-financial-results-reflect-lillys-continued;
JPM 2022: Eli Lilly CEO mulls using Novo's double-branding trick on tirzepatide—one obesity, one diabetes;
Rosenstock J et al. Efficacy and safety of a novel dual GIP and
GLP-1 receptor agonist tirzepatide in patients with type 2 diabetes (SURPASS-1): A double-blind, randomised, phase 3 trial. Lancet 2021 Jun 25; [e-pub]. (https://doi.org/10.1016/S0140-6736(21)01324-6);
Frías JP et al. Tirzepatide versus semaglutide once weekly in patients with type 2 diabetes. N Engl J Med 2021 Jun 25; [e-pub]. (https://doi.org/10.1056/NEJMoa2107519);
等等。
想要解锁更多药企创新药进展信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、最新进展、研发阶段、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包! <END>













收藏
登录后参与评论