中美biotech在策略上完全不同的打法决定了美国式创新之路更坎坷。
2022年刚开局,4款新药研发就收到了受挫,纳斯达克上市的Biotech就有3家抽中了“下下签”。
中国biotech喜欢追求小而全,很多是多个项目同时做,许多小公司虽然pipeline丰富,在做几十个产品,但是没有足够多的资源支撑,因此无法深入做产品。
美国的Biotech注重情报收集,治疗领域分工,避免内卷,侧重在单个领域聚焦,不是小而全,而是小而精,基本上药做first in class的潜力品种,因此风险很大。一旦研发失败,二级市场上股价遭重锤。
开局不利的4款新药,涉及到罕见病、基因治疗、乙肝和中枢神经系统领域。
一、半乳糖血症药物NDA推迟
2022年1月3日 ,
Applied Therapeutics, Inc.(纳斯达克股票代码:APLT)是一家临床阶段的生物制药公司,针对已验证的分子靶标开发一系列新的候选药物,以适应高度未满足的医疗需求,提供了关于
AT-007半乳糖血症计划的监管更新。
在年底与 FDA讨论后,公司决定暂停提交AT-007的NDA用于治疗半乳糖血症,等待与该机构的进一步讨论。尽管先前已在基于减少半乳糖醇的NDA加速批准的背景下讨论了半乳糖血症计划,但 FDA 现在表示可能需要临床结果数据才能获得批准。
受到利空影响,近五个交易日股价大跌超50%。
正在进行的 ACTION-半乳糖血症儿童 3 期研究正在评估 AT-007 治疗与安慰剂随着时间的推移对临床结果的影响,包括认知、言语、行为和运动技能。有防火墙的委员会每 6 个月评估一次临床结果。第一次评估将在 2022 年第一季度完成,之后每 6 个月完成一次,直到研究达到统计学意义。
“虽然对FDA的这一方向改变感到失望,但我们仍然致力于为半乳糖血症患者提供这种重要的治疗方法,”应用治疗学委员会首席执行官、创始人兼主席Shoshana Shendelman 博士说。“我们将继续与FDA合作,确定获得监管批准的最快捷途径,并将相应地提供时间和计划的更新。”
半乳糖血症是一种罕见的遗传代谢疾病,导致无法代谢单糖半乳糖。半乳糖存在于食物中,但也由身体内源性产生。如果代谢不正确,半乳糖会转化为有毒代谢物半乳糖醇,这会导致神经系统并发症,包括语言、认知、行为和运动技能的缺陷,还会导致青少年白内障和卵巢功能不全(女性)。美国大约有 3,000 名半乳糖血症患者,每年有 80 名新生儿。
AT-007是一种中枢神经系统(CNS)渗透性醛糖还原酶抑制剂(ARI),用于治疗几种罕见的神经系统疾病,包括半乳糖血症、SORD缺乏症和PMM2-CDG。在半乳糖血症的动物模型中,AT-007降低了有毒的半乳糖醇水平并预防了疾病并发症。在临床试验中,与安慰剂相比,AT-007显着降低了患有半乳糖血症的成人和儿童的血浆半乳糖醇水平。AT-007目前正在对 2-17 岁患有半乳糖血症的儿童进行 3 期临床结果试验(ACTION-半乳糖血症儿童),以及对患有半乳糖血症的成人进行的长期开放标签研究。AT-007 已获得美国食品和药物管理局 (FDA) 的孤儿药和儿科罕见病指定,用于治疗半乳糖血症和 PMM2-CDG。
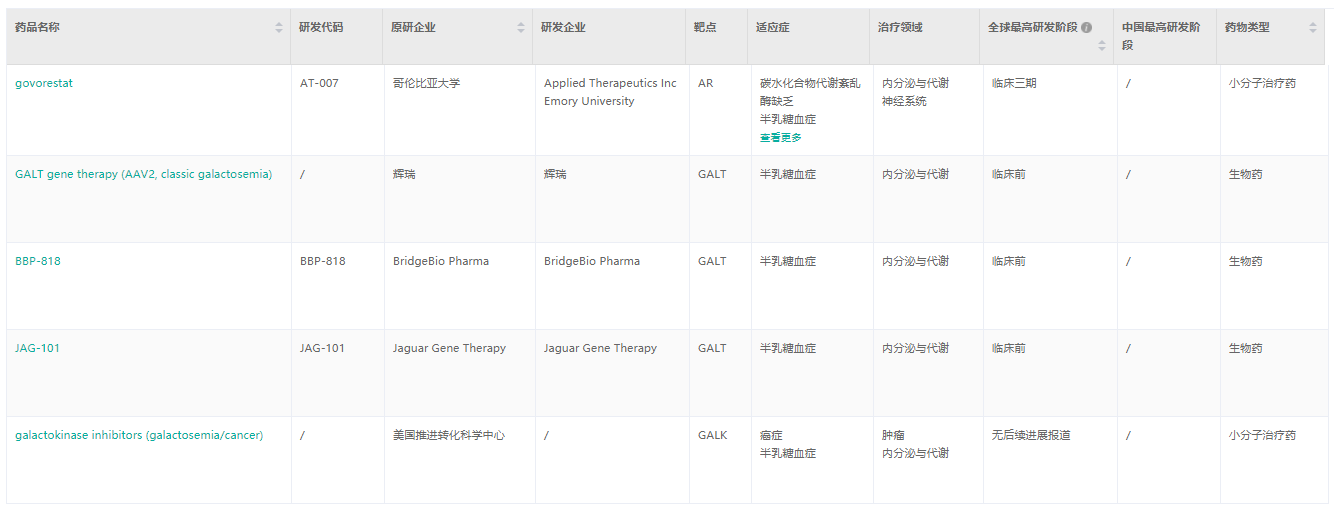
经药融云数据查询,目前在半乳糖血症适应症领域,Applied的AT-007处于最高的研发阶段,其余的还有辉瑞、BridgeBio Pharma、Jaguar Gene Therapy 正在临床前阶段。
半乳糖血症适应症在研药物
截图来源:药融云全球药物研发数据库
二、基因治疗Fabry disease管线停止
1月4日,总部位于马萨诸塞州的基因治疗开发商
Avrobio出人意料地停止其最先进的治疗方法之一的工作,理由是临床试验的结果令人失望,与早期、更有希望的发现形成鲜明对比。在周二的一份声明中,
Avrobio表示将停止招募患者参加一项中期研究,以测试其基因治疗法布里病药物(Fabry disease)(一种罕见的遗传性疾病)——AVR-RD-01,并取消该研究计划的优先级。迄今已接受Avrobio治疗的14名法布里患者将继续监测。
Avrobio在来自最近接受治疗的五名患者中的三名的数据显示该公司治疗旨在产生的关键蛋白质水平下降后做出了决定。据 Avrobio 称,其他结果表明,这种由转基因干细胞组成的疗法并没有像预期的那样在体内扎根,这表明可能对治疗产生抗药性。
受此消息影响,周二股价下跌超过30%。
该公司现在将把重点转移到其针对Gaucher 和胱氨酸病的基因疗法上,这两种疗法都在临床试验中。
由于停止在法布里的工作,Avrobio 现在预计其持有的 2 亿美元现金将持续到 2024 年初。
AVR-RD-01是靶点为GLA,针对法布里病的药物。据药融云数据查询,目前全世界范围内,众多企业都在布局攻克法布里病,现已有赛诺菲、葛兰素史克、日本住友等5款药品上市,其中在中国上市的就有2款,分别是赛诺菲的阿加糖酶β(agalsidase beta)和Excelsior Biopharma IncSK、化工株式会社、日本住友、武田的阿加糖酶α(agalsidase alfa)。另外,在所有针对克法布里病的药物中,GLA靶点为主要靶点,占比64.71%。
法布里病药物研发进展阶段
图片来源:药融云全球药物研发数据库
三、乙肝新药失败,大跌56%
1月6日,临床阶段的生物技术公司
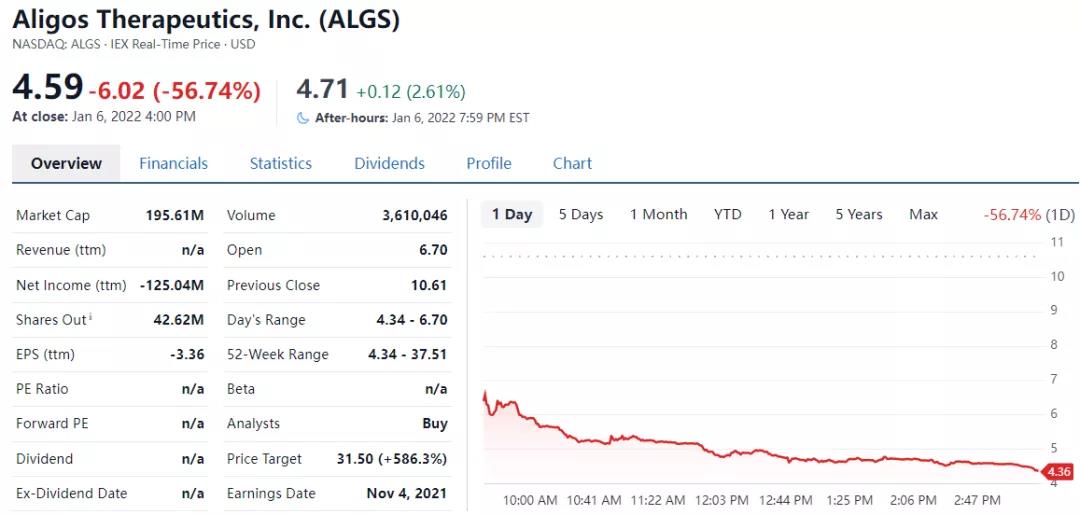
Aligos Therapeutics(纳斯达克股票代码:ALGS)透露,
已经停止进一步开发针对慢性乙型肝炎 (CHB) 的实验药物 ALG-010133。
公司股价当日下跌57%。
该决定是根据该药物 1 期研究的数据做出的,该研究表明,使用 ALG-010133,“在预计的有效剂量下……没有有意义的[乙型肝炎表面抗原]减少”。预计有效剂量(400 mg)的 1 期数据表明抗乙型肝炎病毒的活性不足以证明进一步开发的合理性。
“我们对这项研究的抗病毒活性数据表明 ALG-010133无法对CHB的功能性治愈做出有意义的贡献感到失望,”Aligos 首席执行官 Lawrence Blatt 说。
“乙型肝炎是一种非常具有挑战性的病毒,可能需要涉及不同作用机制的组合方案才能实现功能性治愈,”他补充说。
在承认失败的新闻稿中,Aligos 赶紧指出它还有许多其他治疗方法正在筹备中。
这家成立于2018年并于2020年在证券交易所上市的年轻生物科技公司将继续专注于抗击乙型肝炎和其他肝病,以及各种病毒感染。然而,ALG-010133的退出是一个沉重的打击,显然仍然雄心勃勃的公司需要找到一种方法来恢复。
公司表示,Aligos 的产品线很深,有多种额外的 MOA——ASO、siRNA、CAM I、CAM-2和PD-L1抑制剂——其中许多已经过临床验证,并可能具有同类最佳的特性。具有这些MOA的两种候选药物——ALG-000184(CAM-2)和ALG-020572(ASO)——目前正在临床中,第三个(ALG-125755,siRNA)预计将在 2022 年年中进入临床。
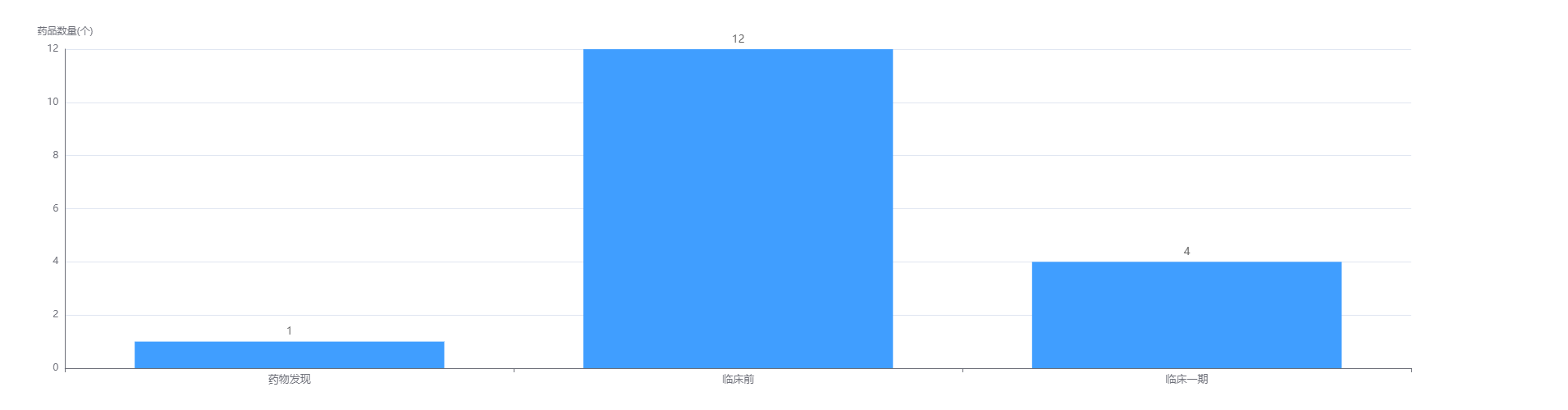
另外,据药融云数据显示,该公司共有17款药物在研发中,其中4款处于临床1期,12款处于临床前。其中,有12款药物都是针对乙肝病毒感染,占比57.15%。可见Aligos在新药研发方面蓄足了力,且专注于乙肝病毒感染药物的研发。
Aligos在研药物研发阶段
图片来源:药融云全球药物研发数据库
四、Modalis停止中枢神经系统新药研发
1月7日,日本上市药企
Modalis Therapeutics Corp宣布,将停止研发一种针对中枢神经系统疾病的新候选药物“
MDL-204”。自 2019 年以来,公司一直在与 Astellas Pharma(安斯泰来)进行联合研究,但经过两家公司的评估,Modalis同意不延长联合研究,因为找不到竞争优势,所以决定不在内部开发它。
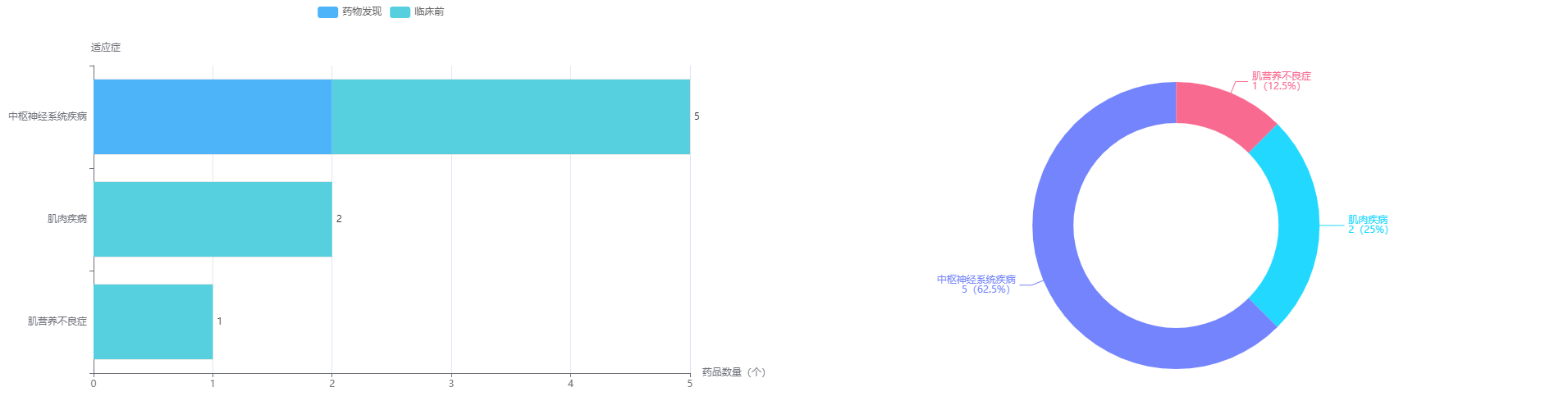
除此之外,Modalis还有4款药物也是针对中枢神经系统疾病的药物,分别是MDL-205、MDL-206、MDL-102、MDL-103,占比62.5%。
Modalis在研药物适用领域
图片来源:药融云全球药物研发数据库
总 结
没有任何商业化产品的生物技术公司在很大程度上依赖于其管道项目的临床试验结果,在美股体现的很明显。
不过,开局“下下签”,早点止损后,进行新的探索,否极泰来,未尝不是好事。
目前中国医药创新也进入了新的阶段,对于FIC的探索可以借鉴欧美日失败的案例,把“下下签”变成“上上签”避免或减少入坑概率。
参考资料:
https://ir.appliedtherapeutics.com/events-and-presentations/events
https://investors.avrobio.com/news-releases/news-release-details/avrobio-reprioritizes-pipeline-programs
https://investor.aligos.com/news-releases/news-release-details/aligos-halting-further-development-stopstm-drug-candidate-alg
<END>
文章来源:药事纵横








收藏
登录后参与评论