据CDE官网公示,广东东阳光药业的1类新药莫非赛定利托那韦片获批临床(默示许可),拟用于治疗慢性乙肝。东阳光药业乙肝新药进展有了更新,现共有5款已步入IND及以上阶段,合力攻坚700亿乙肝市场。
截图来源:CDE官网
莫非赛定利托那韦片是由莫非赛定和利托那韦组成的复方制剂。
其中莫非赛定是由东阳光药业自主研发的、具有独立知识产权的乙肝新药,也是新一代的二氢嘧啶类药物,其作用机制是干扰HBV病毒衣壳体组装,可呈剂量依赖性减少病毒衣壳的正确组装,加速异常衣壳形成,从而强烈抑制乙型肝炎病毒(HBV)的复制及成熟病毒颗粒的产生。
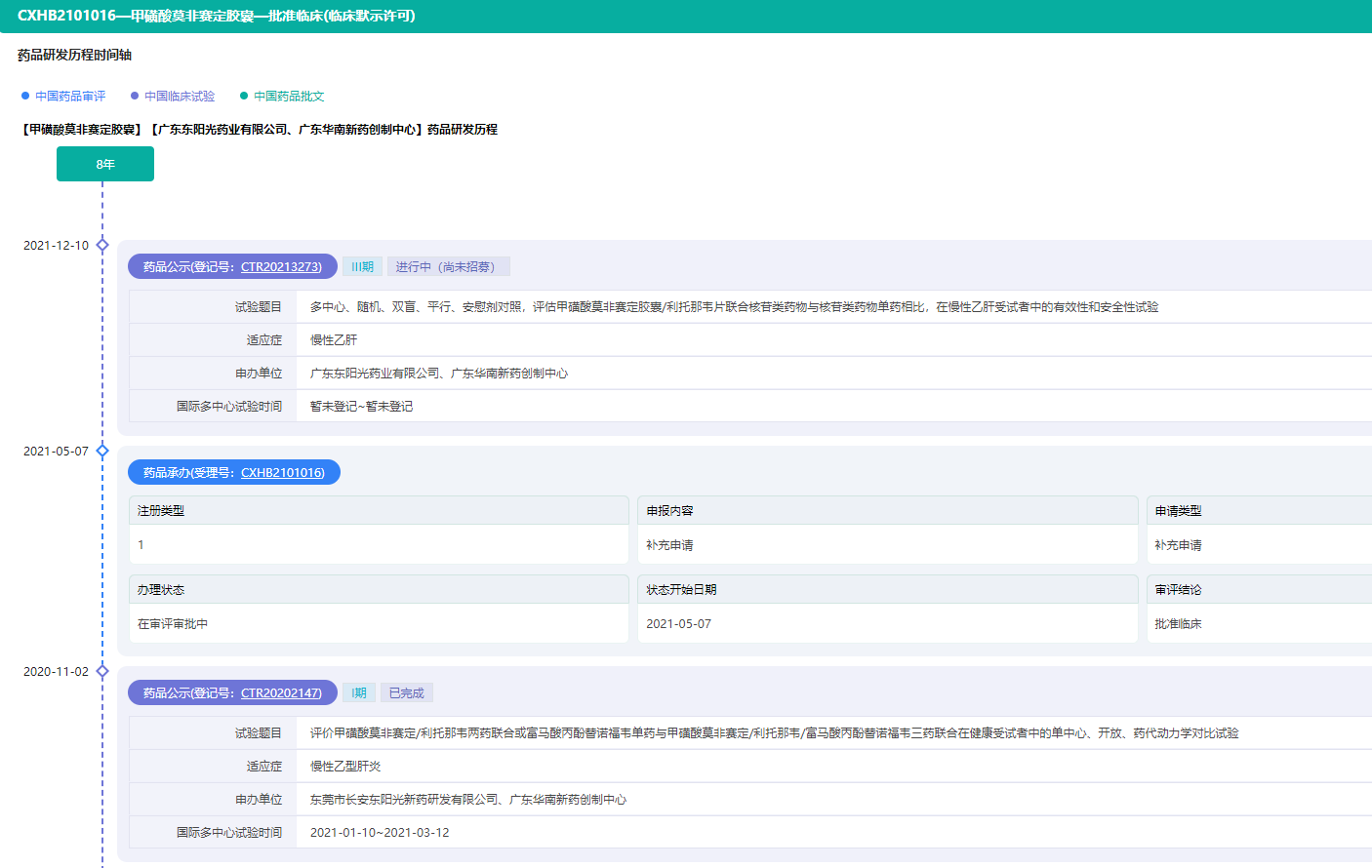
值得注意的是,东阳光药业的甲磺酸莫非赛定胶囊(Morphothiadin ,GLS4)处在Phase III期临床试验阶段,有望2024年上市。这是同靶点在全球范围内研发进展最快的化合物,也是全球首个临床证实可以明确抑制s抗原的小分子化合物。
甲磺酸莫非赛定胶囊药品研发历程时间轴(部分)(微信搜索"药融云小程序"进行相关更多数据查询)
截图来源:药融云中国药品审评数据库
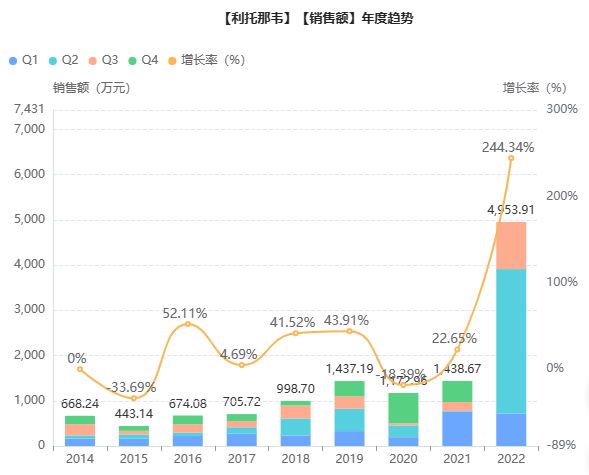
利托那韦则是多种针对病毒蛋白酶的口服抗病毒药物的药代动力学增强剂,临床上主要用于艾滋病的治疗。2022年3月,东阳光药业递交了利托那韦片的仿制上市申请,尚在审评审批中。
近两年有两款含利托那韦的药物获批用于新冠治疗,分别为
辉瑞的
Paxlovid(奈玛特韦片/利托那韦片组合包装)和
海南先声药业的
先诺欣(先诺特韦片/利托那韦片组合包装)。据
药融云数据库,2022年利托那韦相关制剂在院内的销售额出现暴增,前三季度同比增长409%,其中近8成份额来自Paxlovid。
截图来源:药融云全国医院销售数据库
东阳光药业长期布局抗感染领域,在流感、乙肝和丙肝等领域拥有强大的产品管线。东阳光药业的磷酸奥司他韦胶囊、颗粒剂(商品名:可威)是治疗和预防流感的首选用药,磷酸依米他韦胶囊(商品名:东卫恩)作为国内首个自主研发治疗基因1型丙型肝炎的新药,于2021年11月通过国家医保谈判,进入医保目录。
随着时间的推移,全球乙肝新药进展将会不断更新,市场会迎来更多的药物上市。据业内预测,中国乙肝市场将从2025年的156.9亿元增长到2030年的723.3亿元。据查询,除了莫非赛定和莫非赛定利托那韦片外,
东阳光药业还有3款乙肝新药在研:
HEC96719属于FXR 激动剂,针对
乙肝的研究尚在临床前阶段;
哌博赛定属于病毒衣壳抑制剂类药物,处于I期临床试验阶段;
福瑞赛定(HEC-121120)目前正在开展I期临床。
参考来源:
[1] CDE官网
[2] 药融云数据库
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、申报审批情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
—END—










收藏
登录后参与评论