一、6月中国临床试验进展要点
1、6月CDE新公示临床试验共计251项,生物制品56项,中药/天然药物11项,化学药物共计184项,化药占73%
2、药物品种中,依折麦布片、奥贝胆酸片、沙库巴曲缬沙坦钠片和利伐沙班片等药物成最热登记品种
3、从临床分期来看,临床I期74项,临床II期30项,临床III期43项, 临床IV期3项,绝大多数试验处于临床早期阶段
4、从试验状态来看,223项正在进行中,3项试验已完成,其中2项为BE试验
5、新公示BE试验95项,较上月下降5%,浙江诺得药业、常州制药厂和宁波科尔康美诺华药业以3项试验占据BE试验申办单位榜首
6、新公示进口及国内新药147项,强生、阿斯利康、罗氏等多家企业相关药物处于临床后期
7、正大天晴以7项试验位居临床试验申办单位榜首,北京肿瘤医院成最热试验机构
数据统计时间段为2021年6月1日-2021年6月30日,药融云将定期公示临床试验申报信息,关注我们即可定期查看。如有疏漏,欢迎指正!
二、6月公示252项试验,化药占73%非布他司片等药物成最热登记品种
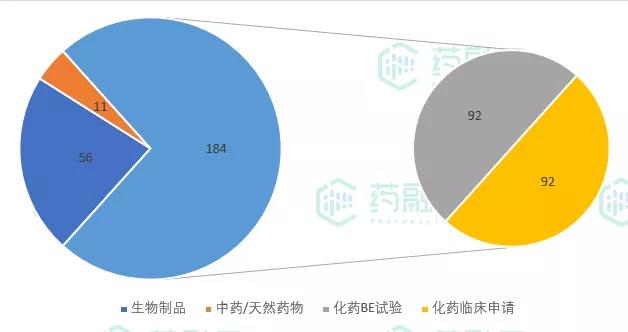
2021年6月1日至6月30日,CDE新公示临床试验共计251项。从药品类型来看,生物制品56项,中药/天然药物11项,化学药物共计184项,占试验总数的73%,其中包括BE试验92项。
6月新公示临床试验药品分类
数据来源:药融云中国临床试验数据库
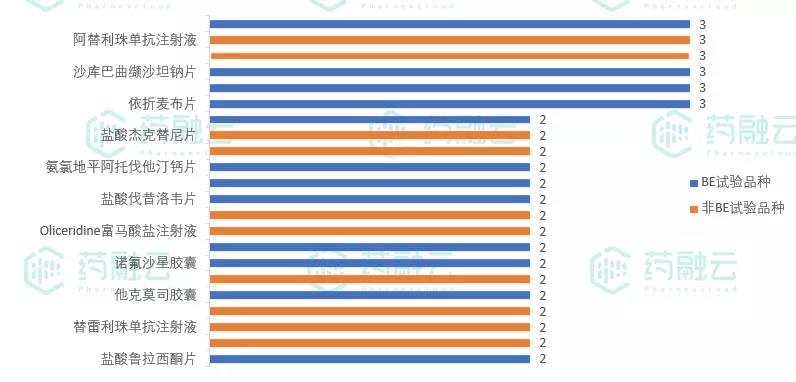
CDE新公示的临床试验药物品种中,共有22个登记试验数≥2的药物品种,其中12项为BE试验品种,依折麦布片、奥贝胆酸片、沙库巴曲缬沙坦钠片和利伐沙班片以3个登记试验位居前列。
登记试验数≥2的药物品种
数据来源:药融云中国临床试验数据库
三、绝大多数试验处于临床早期,三项试验已完成
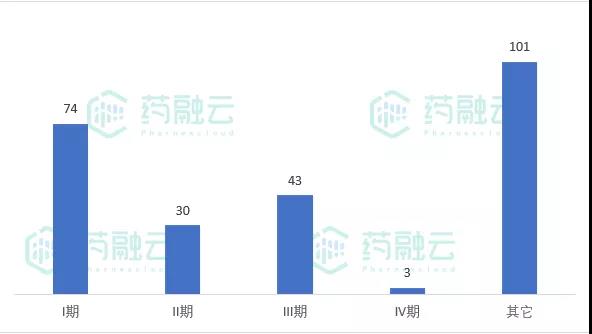
从临床分期来看,临床I期74项,临床II期30项(含I/II期),临床III期43项(含II/III期、I/II/III期), 临床IV期3项,其他试验101项(主要是BE试验)。
6月新公示临床试验分期
数据来源:药融云中国临床试验数据库
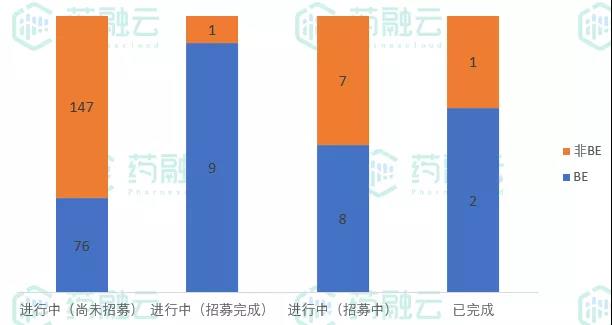
新公示的251项临床试验中,223项正在进行中,3项试验已完成,其中2项为BE试验,涉及上海上药信谊药厂和浙江知一药业。
6月新公示临床试验状态
数据来源:药融云中国临床试验数据库
四、BE试验数较上月下降5%,多家企业申报3项BE试验
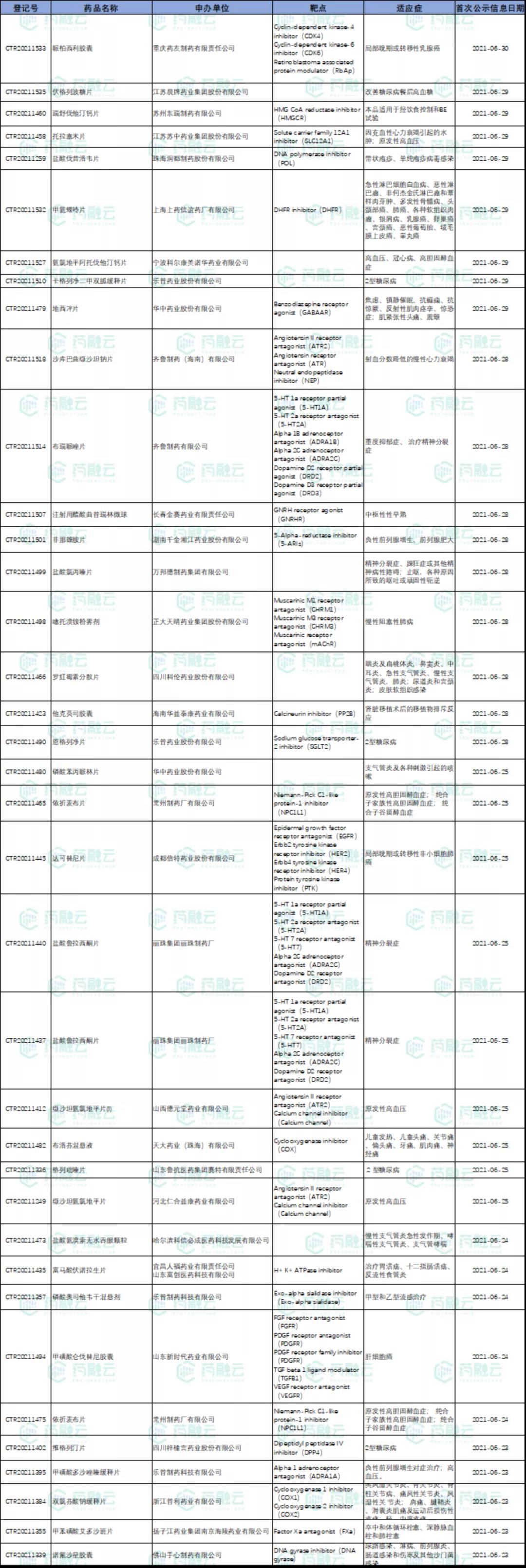
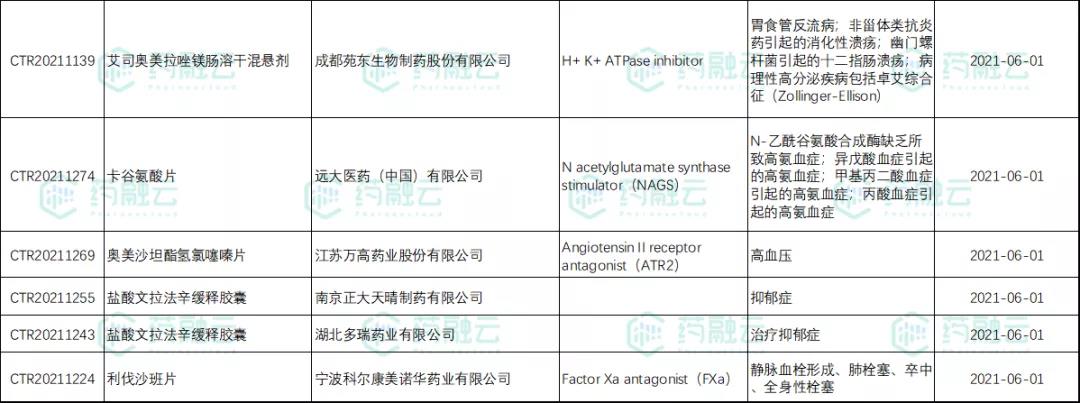
6月新公示BE试验95项,较上月(100项)下降5%。浙江诺得药业、常州制药厂和宁波科尔康美诺华药业以3项试验占据BE试验申办单位榜首。
6月新公示BE试验汇总
数据来源:药融云中国临床试验数据库
数据来源:药融云中国临床试验数据库
五、新公示进口及国内新药147项,强生等企业相关药物处临床后期
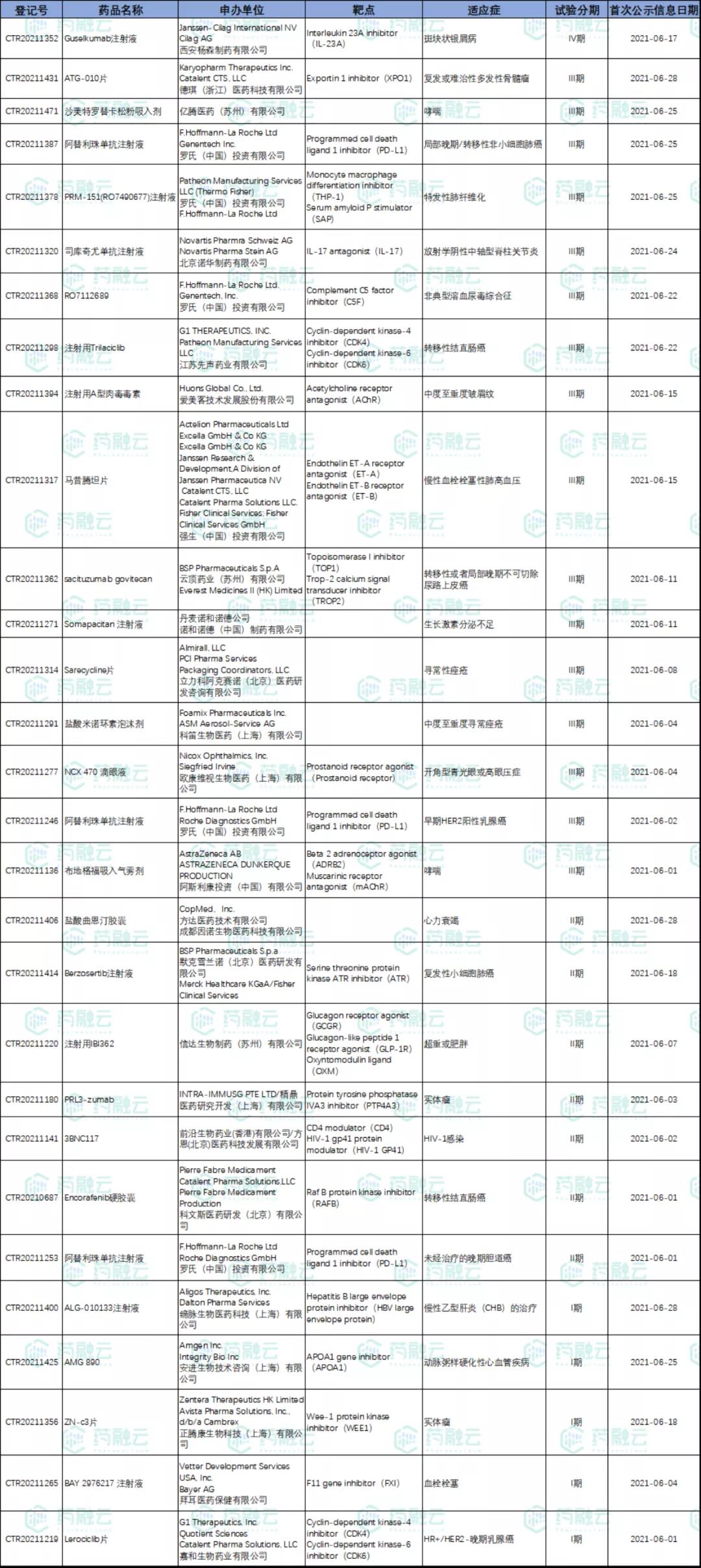
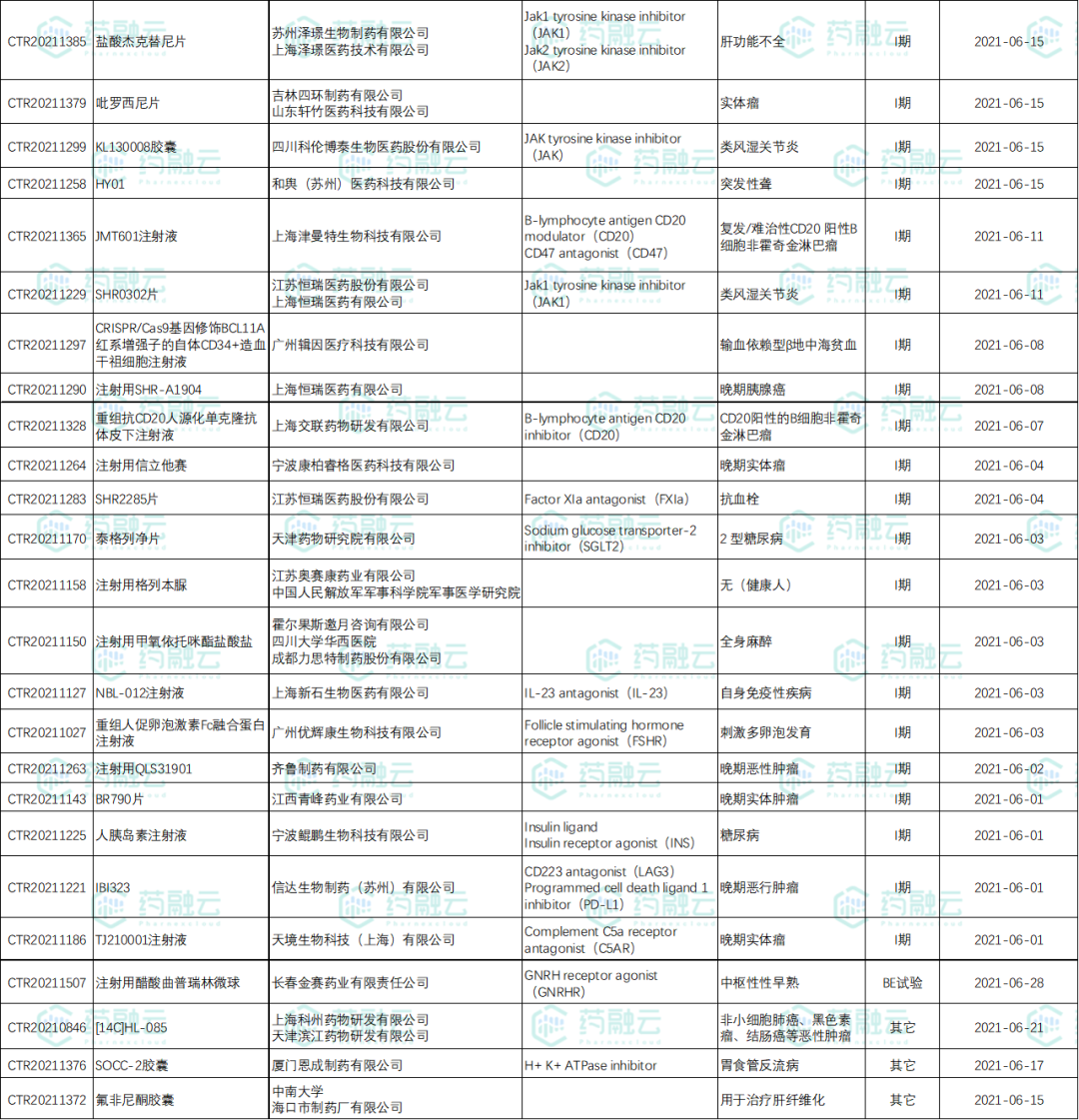
6月新公示进口药试验29项,其中17项试验进入临床III期或IV期,涉及强生、阿斯利康、罗氏等多个企业。
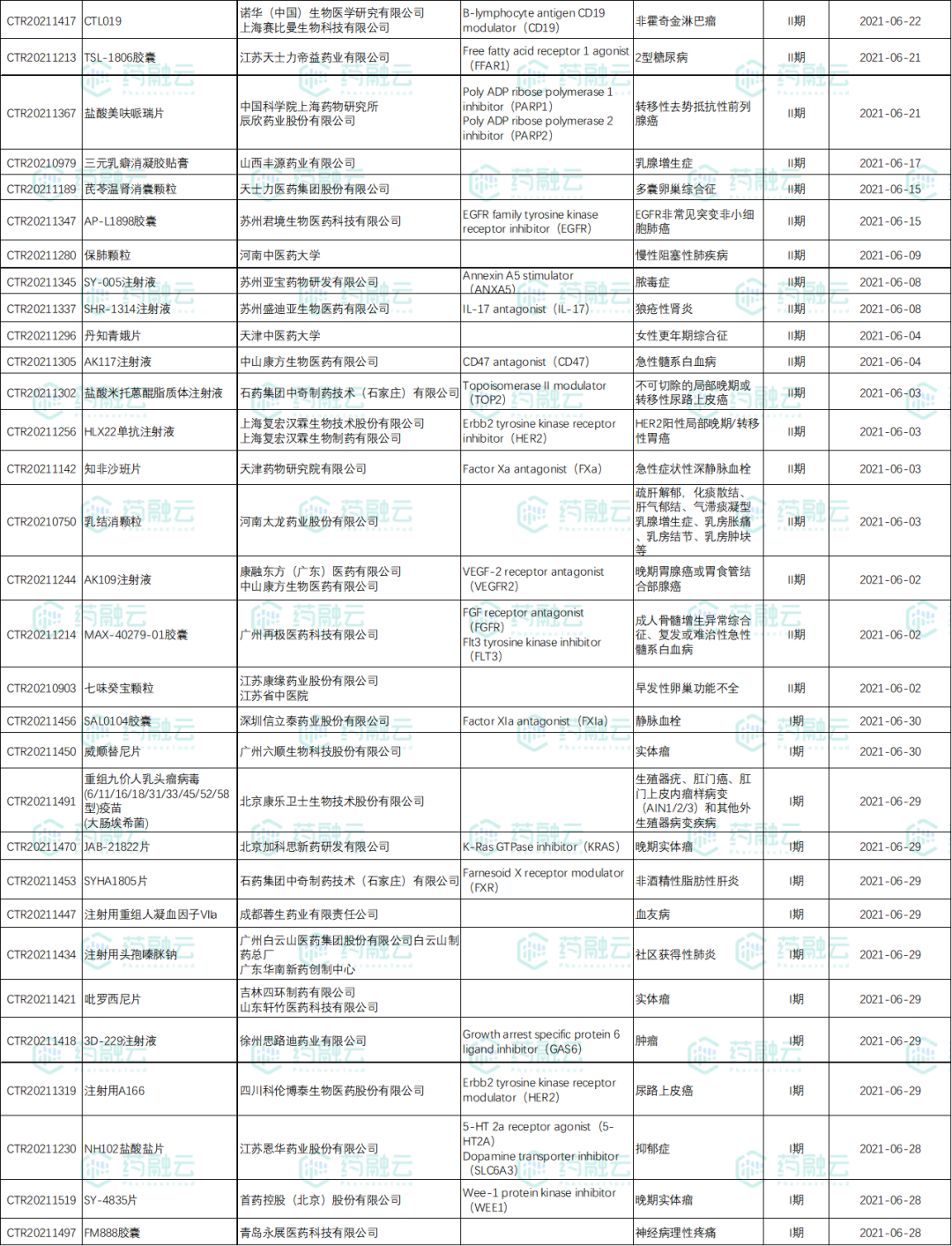
国内新药试验118项,涉及糖尿病、乳腺增生、肿瘤等多个适应症,相比进口药,国内新药仅21%的药物进入临床后期。
6月新公示进口药试验
数据来源:药融云中国临床试验数据库
6月新公示国内新药试验
数据来源:药融云中国临床试验数据库
六、6款重点新药介绍,涉及康方生物、百济神州、罗氏等企业
AK105注射液
申办药企:康方生物
派安普利的Fc受体和补体介导效用功能通过Fc区突变而完全去除,同时具有抗原结合解离速率较慢的特点。这些特点使得派安普利具有更有效地阻断PD-1通路的活性,并维持更强的T细胞抗肿瘤活性,有可能成为临床获益更好的抗PD-1药物。派安普利是中国生物制药唯一可用于开发基于PD-1抗体的单一疗法或联合疗法的新药,也是康方生物处于临床开发后期、具差异化且可能是同类最佳的PD-1单克隆抗体候选药物之一。
BGB-A1217
申报企业:百济神州
BGB-A1217为百济神州开发的一款靶向TIGIT的人源化单克隆抗体,该靶点抑制T细胞/NK细胞介导的肿瘤免疫激活,属于免疫检查点。适应症为晚期实体瘤、食道肿瘤、转移性非小细胞肺癌、鼻咽癌、鳞状细胞癌、子宫颈癌。该款药物是首个进入临床的国内企业开发的TIGIT单抗。
赛沃替尼片
申报企业:和记黄埔
赛沃替尼可选择性抑制MET激酶的磷酸化,对MET14号外显子跳变的肿瘤细胞增殖有明显的抑制作用。该药为我国拥有自主知识产权的创新药,用于含铂化疗后疾病进展或不耐受标准含铂化疗的、具有间质-上皮转化因子(MET)外显子14跳变的局部晚期或转移性非小细胞肺癌成人患者。
阿替利珠单抗注射液
申报企业:罗氏
阿替利珠单抗可通过阻断 PD-L1与其受体PD-1和CD80的相互结合,从而解除肿瘤免疫微环境抑制状态和T细胞耗竭,促进肿瘤特异性T细胞活化、增殖和杀伤效应,进一步杀伤肿瘤细胞。截至目前,阿替利珠单抗可同时用于一线治疗广泛期的小细胞肺癌、联合贝伐珠单抗一线治疗晚期不可切除的肝细胞癌及一线单药治疗PD-L1高表达,且无EGFR或ALK基因突变的转移性非小细胞肺癌。
AB-106
申报企业:葆元生物
AB-106是一款对ROS1及NTRK1-3具有高效抑制作用的双靶点小分子抑制剂。该药安全性好,应答率高,有效持续时间长,能带给病人更长的无疾病进展生存期。另外,AB-106还可穿越血脑屏障,对克唑替尼治疗失败的ROS1阳性非小细胞肺癌患者及脑转移患者也有效。AB-106是新一代广谱抗癌药,有潜力与国际领先的上市明星产品拉罗替尼、恩曲替尼等相媲美。
IBI-323
申报企业:信达生物
IBI-323是信达生物(苏州)有限公司自主研发的1类新药,是同时靶向 PD-L1及LAG-3的双特异性抗体。它在体内的优势主要体现在两个方面:1.同时抑制LAG-3和PD-L1介导的两个抑制性信号通路,具有比单靶点更强且更持久的 T 细胞活化潜力;2.通过双抗的桥接作用,可以将表达PD-L1的肿瘤细胞与表达LAG-3的T细胞拉近,从而形成稳定的TCR:MHC免疫突触,进一步激活T细胞。
七、正大天晴申报试验最多,北京肿瘤医院成最热试验机构
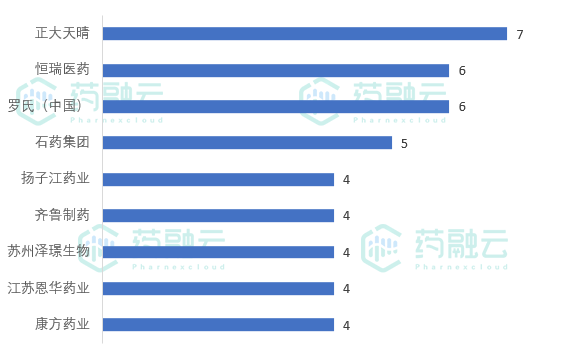
临床试验申办单位中,正大天晴以7项登记试验位居第一。恒瑞、罗氏紧随其后。
临床试验机构中,北京肿瘤医院以8项登记试验高居榜首。
6月临床试验登记数≥4的申办单位
数据来源:药融云中国临床试验数据库
6月临床试验登记数≥4的试验机构




















收藏
登录后参与评论