7月中旬中国临床试验进展要点
1、7月9日-7月18日,CDE新公示临床试验共计104项
2、从药品类型来看,化学药物共计79项,生物制品21项,中药/天然药物4项
3、从临床分期来看,临床I期28项,临床II期12项,临床III期14项
4、从实验状态来看,102项试验在进行中,2项试验已完成
5、BE试验43项,涉及糖尿病、关节炎、高血压等多个适应症,乐普药业、齐鲁制药和华润双鹤药业以2项BE试验并列第一
6、国内外新药试验60项,进口药试验多处于临床后期,涉及罗氏、阿斯利康等企业,国内企业中恒瑞等开展6项试验位列第一
数据统计时间段为2021年7月9日-2021年7月18日,药融云将定期公示中国临床试验进展情况,关注公众号即可定期查看。如有疏漏,欢迎指正!
一、7月9日-7月18日CDE新公示临床试验概览
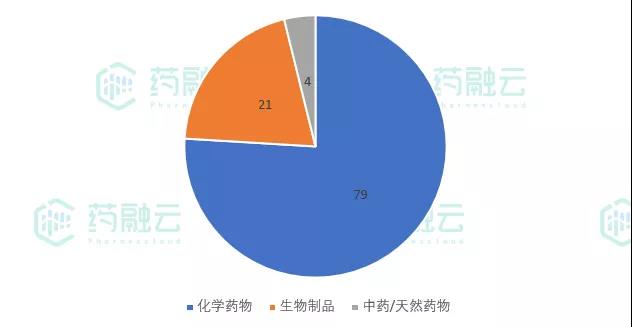
2021年7月9日-7月18日,CDE新公示临床试验共计104项。从药品类型来看,化学药物共计79项,生物制品21项,中药/天然药物4项。
7月9日-7月18日新公示临床试验药品分类
数据来源:药融云中国临床试验数据库
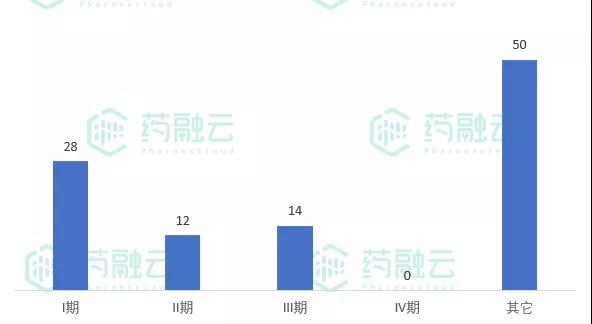
从临床分期来看,临床I期28项,临床II期12项,临床III期14项,临床IV期0项,其他试验50项(主要是BE试验)。
7月9日-7月18日新公示临床试验分期
数据来源:药融云中国临床试验数据库
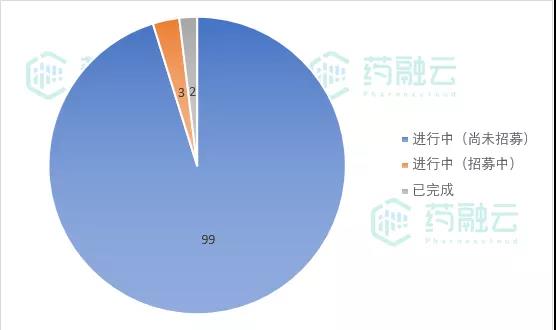
从实验状态来看,102项正在进行中,其中99项尚未招募,3项在招募中。2项实验已完成。
7月9日-7月18日新公示临床试验状态
数据来源:药融云中国临床试验数据库
二、新公示43项BE试验乐普、齐鲁和华润双鹤药业开展最多
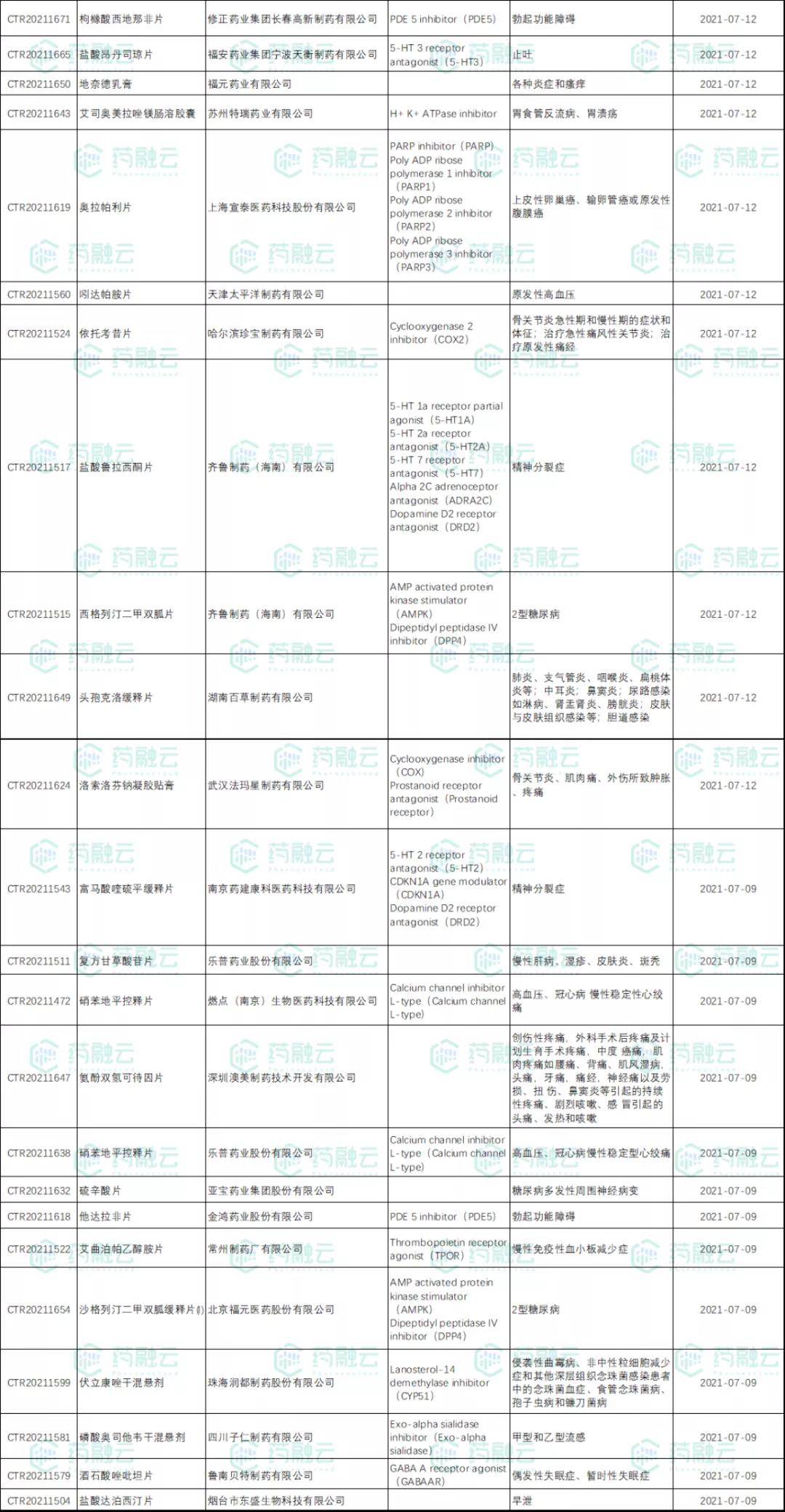
7月9日-7月18日公示BE试验43项,涉及糖尿病、关节炎、高血压等多个适应症。
从试验药品来看,非布司他片、他达拉非片、磷酸奥司他韦干混悬剂和硝苯地平控释片开展最多,均开展2项BE试验。
从申办药企来看,乐普药业、齐鲁制药和华润双鹤药业以2项BE试验并列第一。
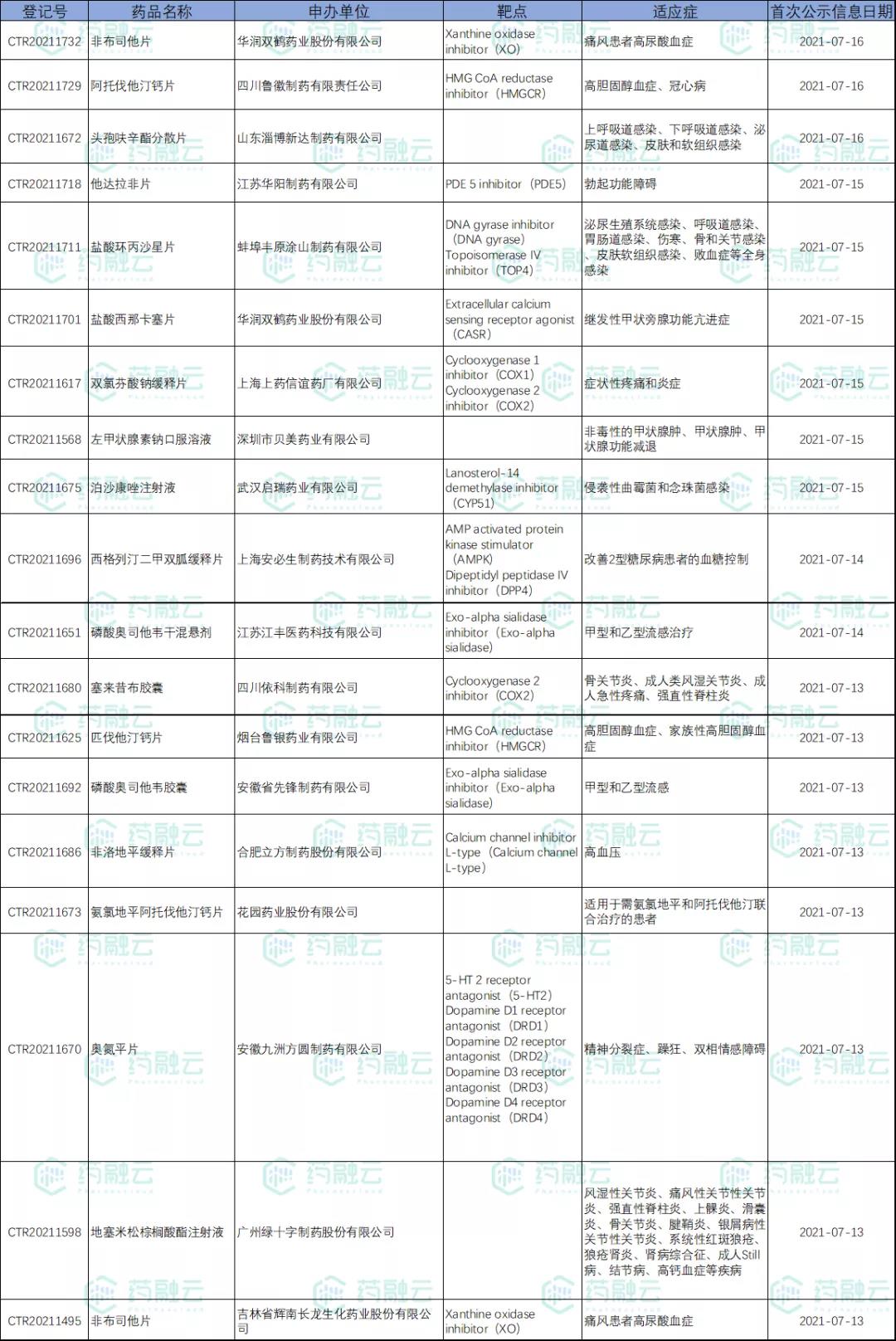
7月9日-7月18日新公示BE试验汇总
数据来源:药融云中国临床试验数据库
三、进口药试验多处临床后期国内企业中江苏恒瑞登记试验最多
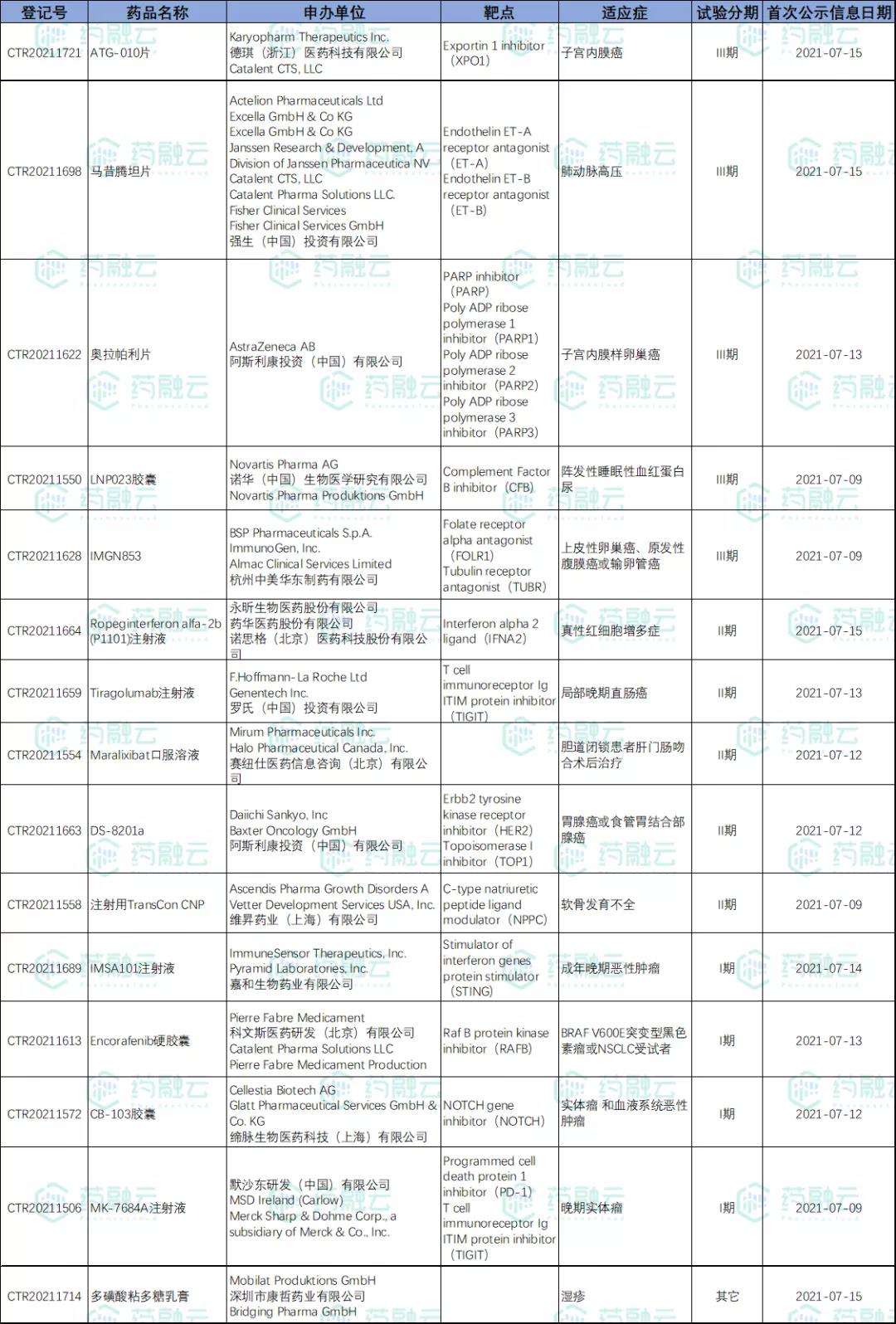
新公示进口药试验15项,其中罗氏、阿斯利康等企业开展的5项试验处于临床III期,涉及子宫内膜癌、恶性肿瘤等适应症。
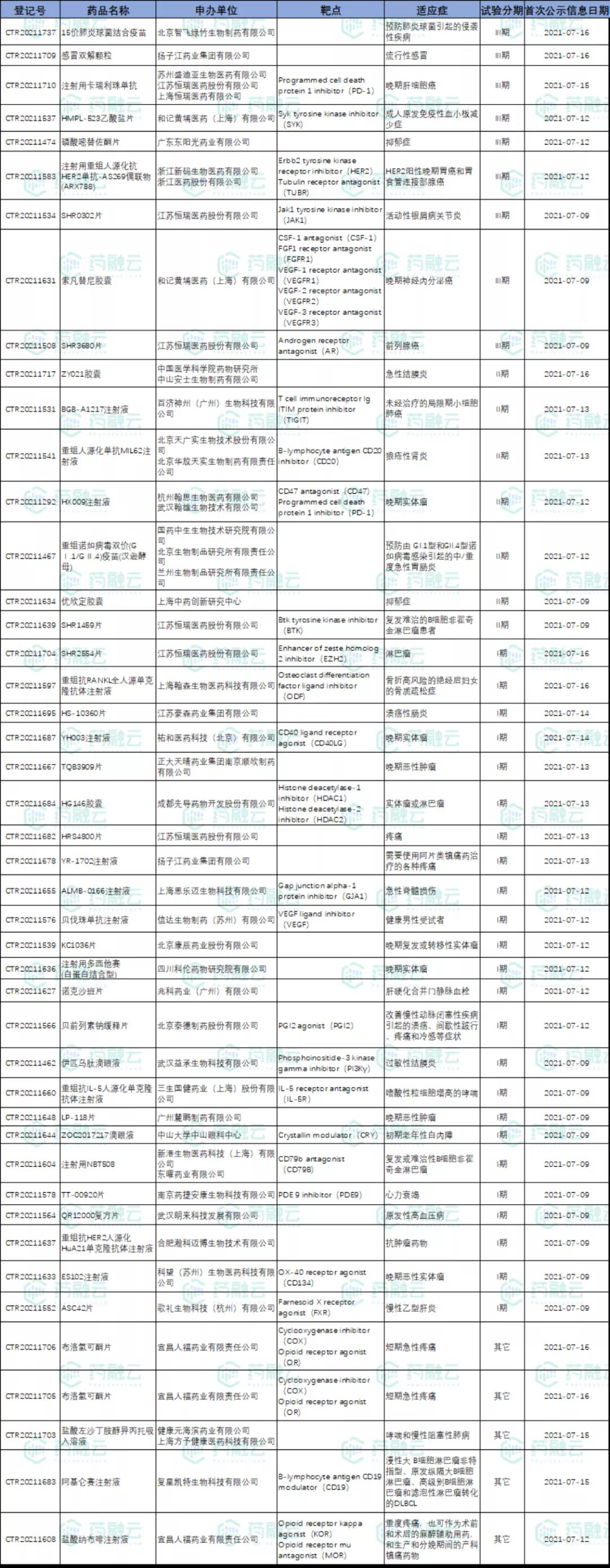
国内新药试验共45项,包括肿瘤、流感等适应症,江苏恒瑞登记试验最多,均开展6项试验。
7月9日-7月18日新公示进口药试验汇总
数据来源:药融云中国临床试验数据库
7月9日-7月18日新公示国内新药试验汇总
四、4款重点新药介绍涉及阿斯利康、恒瑞、罗氏、和记黄埔
阿斯利康——奥拉帕利
奥拉帕利为在我国国内上市的首款 PARP 抑制剂。PARP全称为多聚ADP核糖多聚酶,PARP抑制剂是一种靶向聚ADP核糖聚合酶的癌症疗法。它是第一种成功利用合成致死概念获得批准在临床使用的抗癌药物。简单来讲指的是,当两种不同的基因或蛋白同时发生变化时会导致细胞死亡,而这两种基因或蛋白中如果只有一种异常则不会导致细胞死亡。
江苏恒瑞——SHR-0302
SHR0302是一种高选择性的JAK1抑制剂,可通过抑制JAK1信号传导发挥抗炎和抑制免疫的生物学效应。目前国内外已有JAK1抑制剂获批上市或正在进行不同适应症的临床开发,但尚未有用于特应性皮炎治疗的口服JAK1抑制剂获批上市。该药物与泛JAK抑制剂相比,具有更高的选择性。
和记黄埔——索凡替尼
索凡替尼是由和记黄埔自主研发的一种新型的口服酪氨酸激酶抑制剂,具有抗血管生成和免疫调节双重活性。索凡替尼可通过抑制血管内皮生长因子受体和成纤维细胞生长因子受体以阻断肿瘤血管生成,并可抑制集落刺激因子-1受体,通过调节肿瘤相关巨噬细胞,促进机体对肿瘤细胞的免疫应答。
罗氏——Tiragulumab
Tiragulumab是罗氏重点开发的一款TIGIT免疫检查点抑制剂,TIGIT是肿瘤免疫治疗中最有前景和潜力的靶点之一。研究发现,在多种癌症类型的肿瘤浸润T细胞中,TIGIT都存在高度表达的现象。而且在具有干细胞特征的记忆T细胞中,PD-1和TIGIT均有表达,而LAG-3、TIM-3等其它检查点蛋白并没有在这些细胞中表达。因此,罗氏认为同时靶向PD-L1和TIGIT在逆转传统的T细胞耗竭以外,还有望增加具有干细胞特征的记忆T细胞的数目,从而产生更多的效应T细胞,达到更好的杀伤肿瘤的效果。









收藏
登录后参与评论