6月上旬中国临床试验进展要点
1、从药品类型来看,化学药物共计49项,生物制品18项,中药/天然药物5项
2、从临床分期来看,临床I期16项,临床II期13项,临床III期12项,临床IV期1项
3、从实验状态来看,72项试验均在进行中
4、BE试验29项,利伐沙班片和盐酸文拉法辛缓释胶囊开展最多,南京正大天晴和宁波科尔康美诺华药业有限公司以2项BE试验并列第一
5、国内外新药试验43项,50%进口药试验为肿瘤药物,国内新药试验涉及扬子江、江苏豪森等企业
数据统计时间段为2021年6月1日-2021年6月13日,药融云将定期公示中国临床试验进展信息,关注我们即可定期查看。如有疏漏,欢迎指正!
一、6月1日-6月13日CDE新公示临床试验概览
2021年6月1日-6月13日,CDE新公示临床试验共计72项。从药品类型来看,化学药物最多,共计49项,生物制品18项,中药/天然药物5项。
6月1日-6月13日新公示临床试验药品分类
数据来源:药融云中国临床试验数据库
从临床分期来看,临床I期16项,临床II期(含Ib/II期)13项,临床III期(含II/III期)12项,临床IV期1项,其他试验30项(主要是BE试验)。
6月1日-6月13日新公示临床试验分期
数据来源:药融云中国临床试验数据库
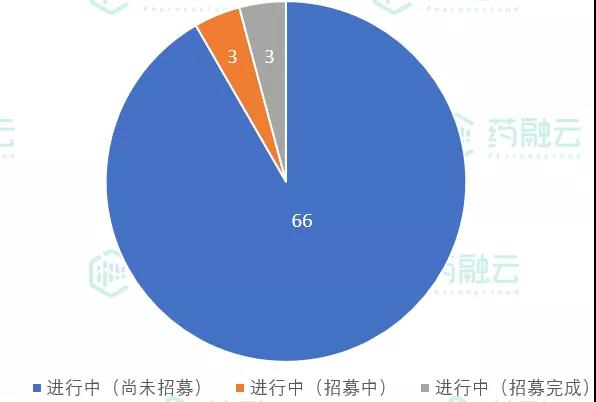
从实验状态来看,72项试验均在进行中,其中66项尚未开始招募,3项试验正在招募中,3项已招募完成。
6月1日-6月13日公示临床试验状态
数据来源:药融云中国临床试验数据库
二、新公示29项BE试验南京正大天晴等开展BE试验最多
6月1日-6月13日公示BE试验29项,涉及高血压、糖尿病、焦虑症等多个适应症。
1、从试验药品来看,利伐沙班片和盐酸文拉法辛缓释胶囊开展最多,分别开展2项BE试验。
2、从申办药企来看,南京正大天晴和宁波科尔康美诺华药业有限公司以2项BE试验并列第一。
6月1日-6月13日新公示BE试验汇总
数据来源:药融云中国临床试验数据库
三、50%进口药试验为肿瘤药物,国内新药试验涉及扬子江等企业
新公示进口药试验12项,其中6项处于临床III期,50%试验药物为肿瘤药物,涉及企业包括诺和诺德、罗氏、阿斯利康等。
国内新药试验共31项,包括肿瘤、糖尿病等适应症,涉及扬子江、江苏豪森、广东东阳光药业等企业。
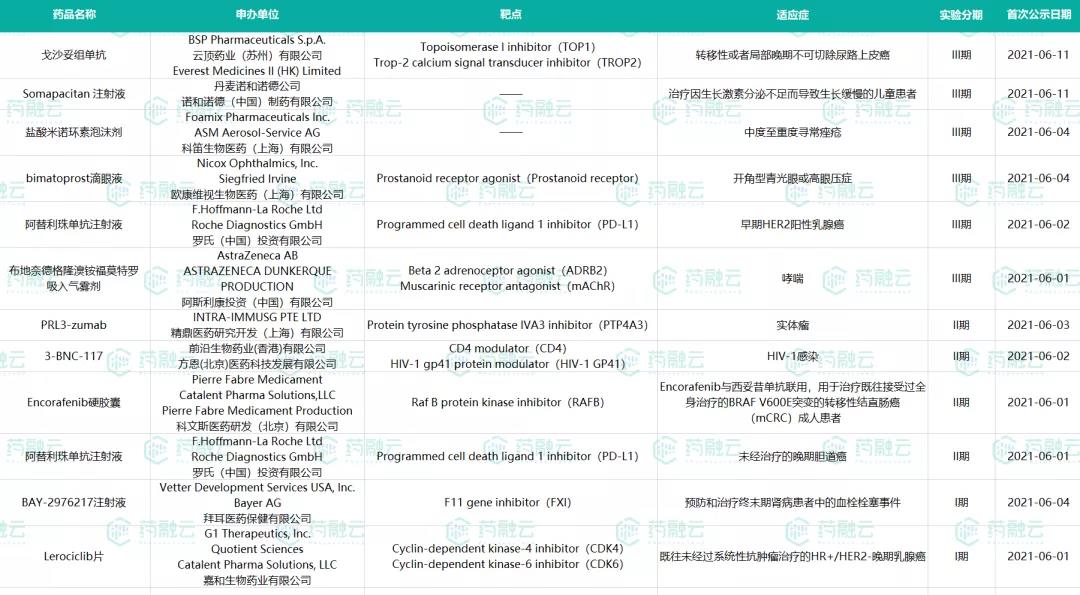
6月1日-6月13日新公示进口药试验汇总
数据来源:药融云中国临床试验数据库
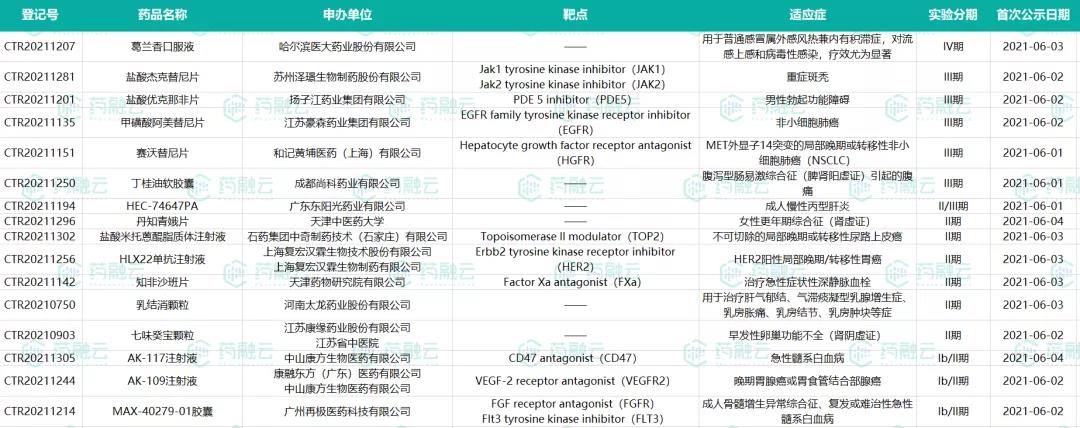
6月1日-6月13日新公示国内新药试验汇总
四、4款重点新药介绍涉及诺和诺德、和记黄埔等企业
Somapacitan注射液
申报企业:诺和诺德
Somapacitan是一种新颖、可逆的、与白蛋白结合的人生长激素衍生物,它由天然的长效人类生长激素(hGH)经过修饰以增强其与内源性血浆蛋白白蛋白的结合,从而延长了分子的半衰期。通过酰化作用向治疗性蛋白质中添加脂肪酸可促进这些分子与循环白蛋白的结合。在人体中,分子与血液中白蛋白的非共价结合会导致清除率降低,并且大大延长了体内半衰期。公开资料显示,Somapacitan已于2020年8月底获美国FDA批准用于生长激素缺乏症(GHD)成年患者,成为首款每周仅需在皮下注射一次的hGH疗法。
戈沙妥组单抗
申报企业:云顶药业等
戈沙妥组单抗是一款靶向Trop-2的新型、首创的抗体偶联药物(ADC),由靶向TROP-2抗原的人源化IgG1抗体与化疗药物伊立替康的代谢活性产物SN-38偶联而成,药物-抗体比高达7.6:1。Trop-2是一种在许多上皮性肿瘤中频繁表达的细胞表面蛋白,包括转移性三阴性乳腺癌(TNBC)和转移性尿路上皮癌(UC),其高表达与高复发率和低生存率相关。戈沙妥组单抗与Trop-2靶向结合并递送抗癌制剂SN-38来杀死癌细胞。云顶新耀近日宣布,中国国家药品监督管理局(NMPA)已受理戈沙妥组单抗的生物制品上市许可申请,用于治疗先前已接受过至少2种系统疗法、其中至少1种疗法治疗转移性疾病的不可切除性局部晚期或转移性三阴性乳腺癌(mTNBC)成人患者。
赛沃替尼片
申报企业:和记黄埔
赛沃替尼片是和记黄埔自主研发的一款高选择性c-Met抑制剂,已于2017年3月获药监局授予突破性疗法资格,用于治疗胃癌、乳头状肾细胞癌以及非小细胞肺癌。在中国,赛沃替尼治疗MET 14外显子跳跃突变非小细胞肺癌的上市申请已纳入优先审评。据悉,这是赛沃替尼在全球的首个新药上市申请,也是中国首个选择性MET-TKI的新药上市申请。
AK-117注射液
申报企业:中山康方
AK117是康方生物自主研发的新型抗CD47单克隆抗体。CD47高表达于多种肿瘤细胞,通过与巨噬细胞表面的SIRPα结合释放“别吃我”信号,抑制巨噬细胞的吞噬作用。靶向CD47药物单药和联合治疗在血液肿瘤和实体瘤中均显示出良好的抗肿瘤疗效,是下一代肿瘤免疫治疗的热门靶点。然而,由于CD47在红细胞表面的广泛表达,靶向CD47药物可导致红细胞的吞噬破坏和凝集,影响其使用的安全性和耐受性。AK117通过其独特的结构,在保留抗肿瘤活性同时,消除了红细胞凝集作用,并显著降低其介导的巨噬细胞对红细胞吞噬活性,有望成为临床获益更好的抗CD47药物。















收藏
登录后参与评论