5月22日,CDE官网显示,正大天晴的1类化药新药TQ-B3525片申报上市并获CDE受理。这是国内第一款报上市的PI3Kα/δ双重抑制剂,同时也是全球第一款,非常值得关注。
截图来源:CDE官网
据
药融云数据库显示,TQ-B3525片是一种全新化学结构的1类
抗肿瘤新药,为新型PI3Kα/δ双重抑制剂,可克服单独抑制PI3Kδ亚基时引起的PI3Kα亚基活性上调而引发的耐药问题。目前,该药在中国多项肿瘤相关临床正在进行中。
TQ-B3525药物研发信息(部分,完整内容请登录“药融云数据库www.pharnexcloud.com/?mh”查看)
截图来源:药融云全球药物研发数据库
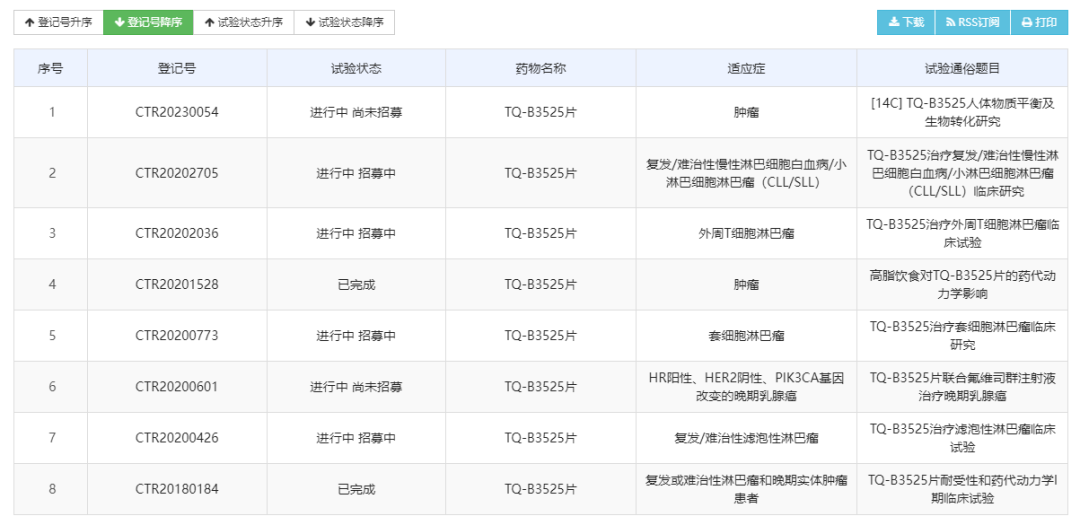
根据药物临床试验登记与信息公示平台显示,TQ-B3525在药监局已登记了多项临床试验,包括:
- TQ-B3525治疗复发/难治性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)临床研究
- TQ-B3525片联合氟维司群注射液治疗晚期乳腺癌
2021年7月,TQ-B3525片获药监局同意纳入突破性治疗药物程序,拟定适应症为:既往至少二线治疗失败的复发/难治滤泡性淋巴瘤治疗。
经药融云数据库查询显示,在全球范围内,鲜有药企布局PI3Kα/δ双重抑制剂,特别是在国内,仅正大天晴一家。此次,正大天晴递交新药上市申请,若顺利获批,不仅是国内第一款PI3Kα/δ双重抑制剂,同时也会成为全球第一款PI3Kα/δ双重抑制剂,在药物研发领域建立起一座里程碑。
截图来源:药融云全球药物研发数据库
参考来源:
[1] CDE官网
[2] 药融云数据库
[4] 药物临床试验登记与信息公示平台
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
<END>









收藏
登录后参与评论