11 月 24 日,诺和诺德表示,将于明年2 月 22 日在日本推出其广受欢迎的减肥神药 Wegovy。
Wegovy由诺和诺德于2012年研发,2021年6月首次在美国上市,成为第一个也是唯一一个被批准用于肥胖症患者体重管理的每周一次
GLP-1受体激动剂。同年该药在中国内地市场获批用于2型糖尿病治疗。
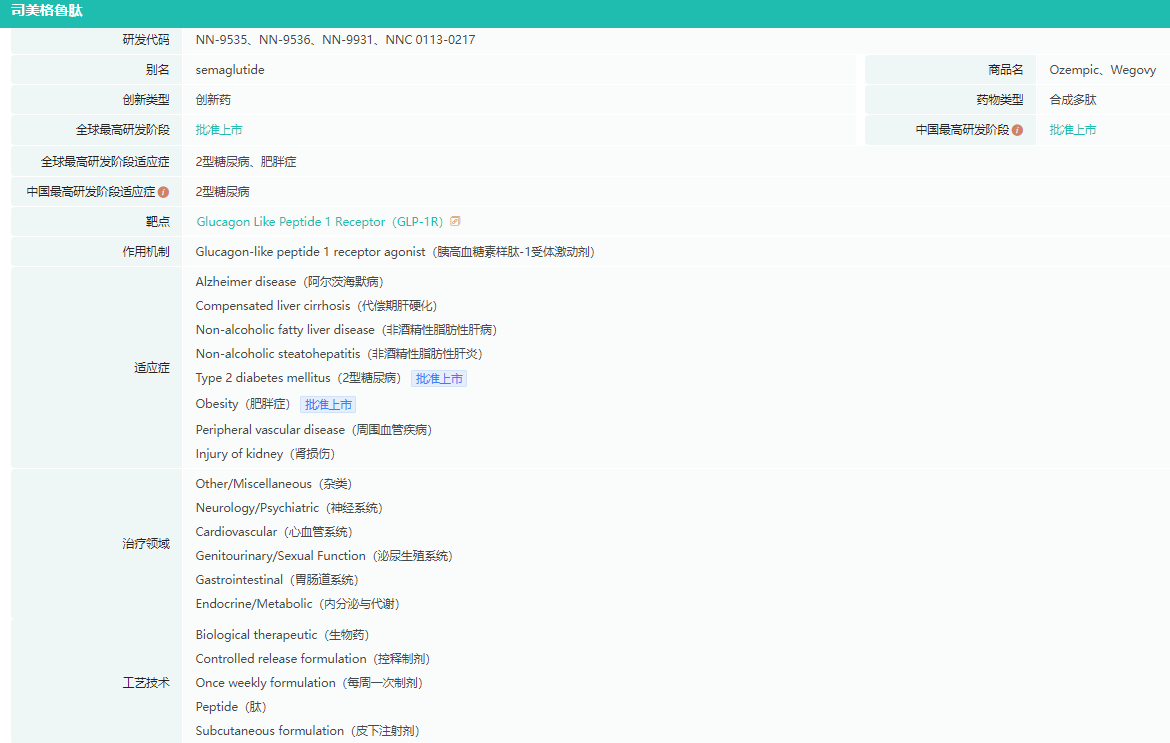
Wegovy药物基本信息
截图来源:药融云全球药物研发数据库
Wegovy上市国家及费用如下:
- 美国:约1350美元/月(不考虑剂量价格差异)
- 丹麦:2370.60丹麦克朗/月(约348美元)
- 挪威:2775.30挪威克朗/月(约258美元)
- 德国:301.91欧元/月(约330美元)
- 英国:未公开
注:1 丹麦克朗 ≈ 0.1468 美元,1 挪威克朗 ≈ 0.0931 美元,1 欧元 ≈ 1.0941 美元
这是该药首次在亚洲上市,迄今为止,Wegovy已在美国、英国、德国、挪威及其本土市场丹麦上市。
尽管与西方国家相比,亚洲国家肥胖问题要小得多。日本是世界上肥胖率最低的国家之一。根据全球肥胖观察站的数据,2019 年,日本只有 4.5% 的成年人处于肥胖状态(BMI ≥30)。
诺和诺德表示,当日本患者的BMI>35,或患有两种及以上肥胖相关合并症的患者的BMI>27,则可以使用Wegovy。
Wegovy有五种不同剂量,分别为0.25mg、0.5mg、1.0mg、1.7mg和2.4mg。在日本,0.25mg的Wegovy每月使用费用为7504日元(约50美元,按1 日元 ≈ 0.0067 美元计算),2.4毫克的Wegovy每月使用费用为42960日元(约287美元)。
大多数日本患者将为 Wegovy 自费 30% 的医疗费用,与其他药物的报销一致。诺和诺德正试图说服政府为一些严重超重的患者支付 Wegovy 费用。
值得注意的是,11月23日,法新社巴黎报导,
面对司美格鲁肽供应瓶颈的挑战,诺和诺德将投资21亿欧元(约23亿美元)来扩大其在法国的生产。
法国总统马克龙将于周四晚些时候在该公司位于巴黎西南部Chartres的工厂主持启动仪式。该工厂将创造500个就业岗位。
参考资料:
药融云数据库
https://www.novonordisk.com/news-and-media/news-and-ir-materials/news-details.html?id=166350
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!







收藏
登录后参与评论