 3月9日,诺和诺德的减重疗法Wegovy(semaglutide,司美格鲁肽)获得FDA新适应症的批准。司美格鲁肽成为获批用于辅助患有心血管疾病及肥胖或超重的成年人预防重大心血管事件的首款减重药物。
3月9日,诺和诺德的减重疗法Wegovy(semaglutide,司美格鲁肽)获得FDA新适应症的批准。司美格鲁肽成为获批用于辅助患有心血管疾病及肥胖或超重的成年人预防重大心血管事件的首款减重药物。
2023年11月,诺和诺德公布了司美格鲁肽对心血管健康的影响,并公布了III期SELECT试验的结果。与安慰剂相比,在标准治疗的基础上注射2.4毫克Wegovy可使主要心血管不良事件减少20%。
FDA药物评估与研究中心糖尿病、血脂紊乱和肥胖症处处长John Sharretts 表示:"Wegovy现在是首款获准用于帮助患有心血管疾病、肥胖或超重的成年人预防危及生命的心血管事件的减肥药,这类患者心血管死亡、心脏病发作和中风的风险较高。提供一种被证明能降低这种心血管风险的治疗方案是公共卫生方面的一大进步"。
上市及销售情况
司美格鲁肽注射液2型糖尿病适应症及减重适应症分别于2017年和2021年由FDA获批上市,商品名分别为Ozempic及Wegovy。从减重开始,司美格鲁肽的适应症不断拓展,此后在心脏病、中风、慢性肾病等领域适应症临床研究均传来好消息。目前司美格鲁肽治疗NASH、阿兹海默症、心衰、外周动脉疾病等适应症均已进入3期临床阶段,前景值得期待。
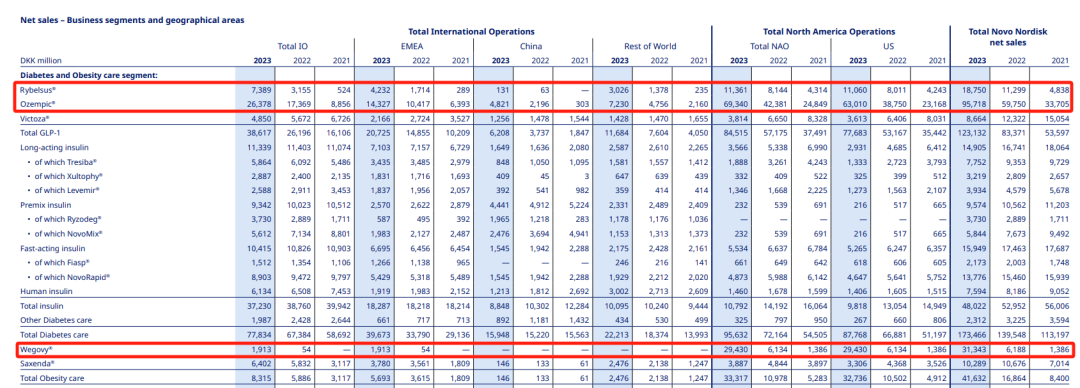
诺和诺德报告称:由于其GLP-1药物销售强劲,2023年利润大幅飙升。司美格鲁肽2023年全年总销售额已达到1458.11亿丹麦克朗,约212.0亿美元,是公司最大的“印钞机”。其中Rybelsus(口服司美格鲁肽)2023年卖出187.50亿丹麦克朗(约合27.21亿美元),Ozempic(注射司美格鲁肽)卖出957.18亿丹麦克朗(约合138.92亿美元),Wegovy(减肥版司美格鲁肽)也卖出313.43亿丹麦克朗(约合45.49亿美元)。
总结
目前,诺和诺德针对GLP-1类药物正在开发慢性肾病、非酒精性脂肪性肝炎、阿兹海默症等多种慢性病适应症,目前司美格鲁肽治疗非酒精性脂肪性肝炎、阿兹海默症、射血分数保留的心衰(HFpEF)、外周动脉疾病等适应症均已进入3期临床阶段。随着GLP-1类药物在多项前期临床研究中展现积极性结果以及相关基础研究的进一步深入,未来GLP-1类药物有望让更多适应症人群得到有效治疗。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!













收藏
登录后参与评论