
今年,各大制药公司都在为专利到期做准备,这将对全球最畅销的几款药品产生重大影响。根据Allied Market Research的报告,2022年全球专利药市场规模为8,144亿美元,预计到2032年将达到14,565亿美元。英国市场情报公司EvaluatePharma的一份报告显示,由于药物的关键专利预计将在2018年至2024年期间到期,可能使全球制药公司价值2510亿美元的品牌药品销售额化为乌有。
专利到期前1-2年是药品生命周期中的重要时期。原研药企和仿制药企都需要制定应对策略,以应对市场变化和新机遇。这也给医药企业营销、研发等部门带来新的挑战。
以下是2024年专利到期的10款重磅药物:
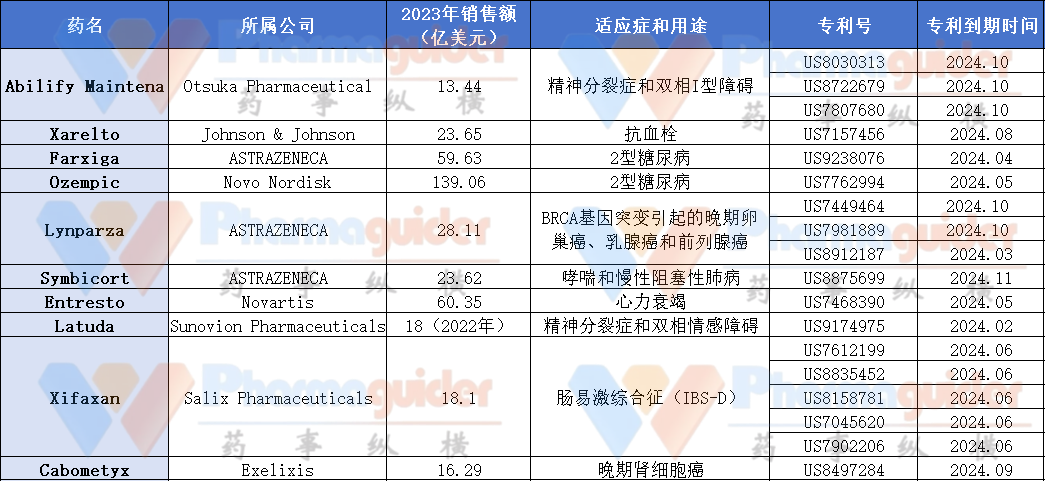
1、Abilify Maintena (Aripiprazole,阿立哌唑长效肌内注射剂) :

Abilify Maintena是由大冢制药(Otsuka Pharmaceutical)和灵北制药联合研发的一款长效注射型抗精神病药物,2013年上市后,Abilify Maintena成为患者和医生治疗精神分裂症的重要选择。Abilify Maintena 2023年销售额为13.44亿美元,该药部分专利将于2024年10月到期。
Abilify Maintena作为每月一次的肌内注射(IM)剂型药物,用于精神分裂症的成人治疗和双相情感障碍I型的成人维持治疗,目前尚不清楚Abilify Maintena对于18岁以下儿童是否安全有效。该药于2013年在美国上市用于治疗精神分裂症,随后在50多个国家上市。2017年,该产品在美国和加拿大被批准用于治疗双相I型障碍。2015年在日本上市用于治疗精神分裂症,并于2020年被批准用于双相I型障碍的附加适应症。2023年5月在中国获批用于精神分裂症的治疗。专家认为,Abilify Maintena有望继续主导这一不断增长的抗精神病药物市场。

图片来源:Otsuka财报
2、Xarelto(Rivaroxaban,利伐沙班):

由杨森制药公司开发的Xarelto是全球用药最广泛的非维生素K拮抗剂口服抗凝剂(NOAC),是抗凝药物市场上最畅销的药物之一,2023年全年销售额23.65亿美元,部分专利将于2024年8月到期。
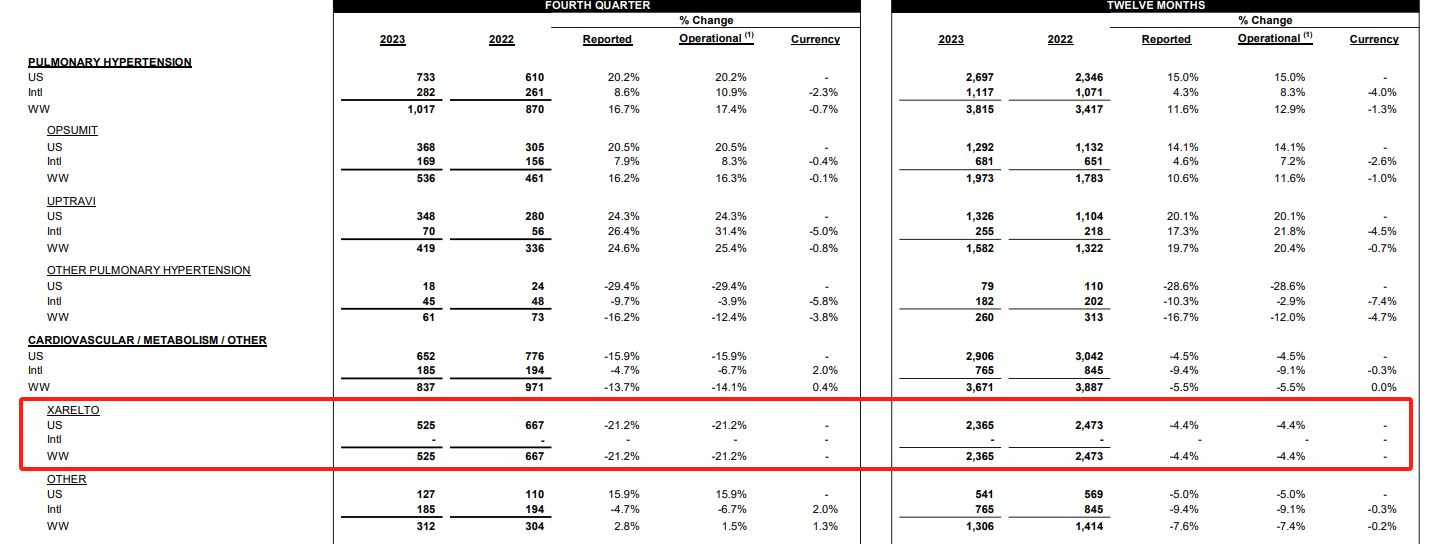
图片来源:强生财报
Xarelto是一种口服生物可利用因子Xa抑制剂选择性阻断因子Xa的活性位点和为活性不需要辅助因子(例如抗凝血酶[抗-thrombin]III)。因子X的激活因子Xa(FXa)通过内源和外源通路在血液凝固级联反应中起中心作用。Xarelto适用于降低非瓣膜性心房颤动患者中风和全身性栓塞的风险,还可用于预防膝关节或髋关节置换手术后可能导致肺栓塞的深静脉血栓形成。
3、Farxiga(Dapagliflozin,达格列净):
AstraZeneca公司的Farxiga是抗糖尿病药物中的佼佼者,自上市以来Farxiga已成为该公司的糖尿病特效药,2023年销售额约为59.63亿美元,部分专利将于2024年4月到期。
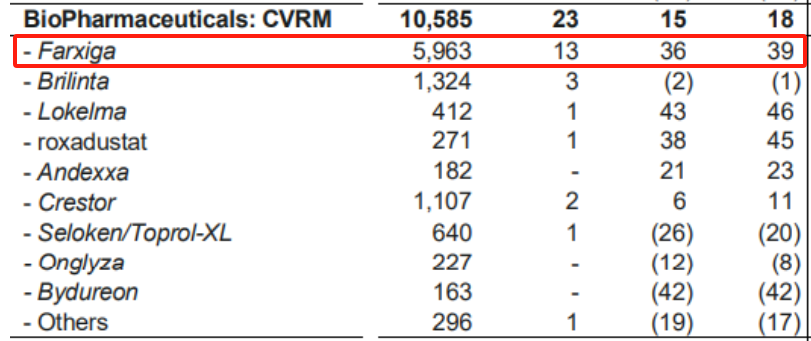
图片来源:阿斯利康财报
Farxiga是一种首创的、每日口服一次的选择性钠葡萄糖协同转运蛋白2(SGLT2)抑制剂,用于改善成人2型糖尿病患者的血糖控制,既可作为单一疗法,也可作为附加疗法,但也存在尿路感染等副作用。
4、Ozempic(Semaglutide,注射用司美格鲁肽):
诺和诺德开发的Ozempic是一款可注射的长效胰高血糖素样肽-1受体(GLP-1R)激动剂,用于改善2型糖尿病患者的血糖控制。自获批以来,Ozempic已迅速成为诺和诺德的糖尿病重磅药物,2023年销售额约139.06亿美元,该药部分专利将于2024年5月到期。

图片来源:诺和诺德财报
2017年12月,司美格鲁肽注射液(商品名为Ozempic)获得美国食品药品监督管理局(FDA)批准上市,用于成年2型糖尿病患者控制血糖。2021年4月,Ozempic获得我国食品药品监督管理局(NMPA)批准上市,用于治疗成人2型糖尿病及降低T2DM合并心血管疾病患者的心血管不良事件风险,并得以进入医保。
Ozempic在全球28个国家中申请了227项专利,可以说有着强大的专利丛林保护。鉴于Ozempic的超强吸金能力,仿制药制造商似乎特别渴望在GLP-1 药物的专利丛林中大刀阔斧。仿制药制造商已经提起了至少24 起专利挑战诉讼。Viatris已经向FDA提交了他们的仿制药商业化申请,但今年1月遭到了诺和诺德的起诉。
5、Lynparza (Olaparib,奥拉帕利):

随着非传染性疾病(NCD)的负担日益加重,癌症治疗市场也在持续增长。AstraZeneca的Lynparza就是这样一款药物,在2023年创造了28.11亿美元的销售额,该药部分专利将于2024年10月和3月到期。
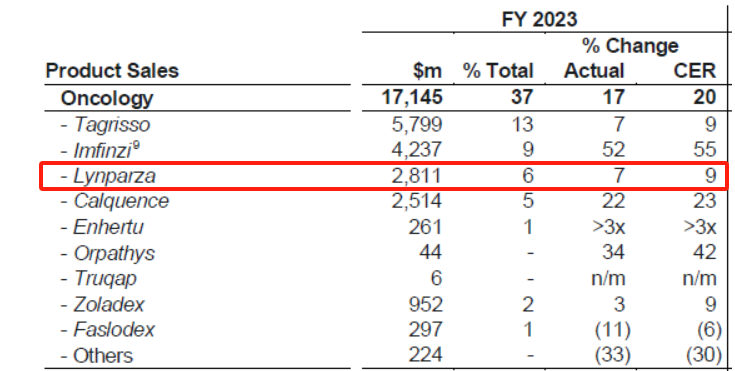
图片来源:阿斯利康财报
Lynparza是一种聚ADP-核糖聚合酶 (PARP) , PARP1和PARP2的选择性强效抑制剂,自2014年首次获批以来,Lynparza已成为BRCA基因突变患者的重要治疗手段。
Lynparza由阿斯利康和默沙东(MSD)联合开发和商业化,作为同类首创的PARP抑制剂,也是第一个阻断细胞/肿瘤中DNA损伤反应(DDR)的靶向治疗,其拥有广泛的临床试验开发计划。奥拉帕利已在国内获批多个适应症,包括铂敏感的复发性卵巢癌、输卵管癌或原发性腹膜癌的维持治疗、乳腺癌易感基因(BRCA)突变的晚期卵巢癌、输卵管癌或原发性腹膜癌的一线维持治疗、BRCA突变且在既往新型激素药物治疗后出现疾病进展的转移性去势抵抗性前列腺癌单药治疗。
6、Symbicort(budesonide and formoterol fumarate dihydrate,信必可都保)
阿斯利康开发的Symbicort是哮喘和慢性阻塞性肺病等呼吸系统疾病领域的重要药物。自 2006年在美国上市以来,信必可已成为阿斯利康最成功的呼吸系统药物之一。该药2023年销售额23.62亿美元,部分专利将于2024年11月到期。

图片来源:阿斯利康财报
Symbicort是一款用于治疗哮喘及慢性阻塞性肺病(COPD)的联合药物,其成分包括糖皮质激素布地奈德(Budesonide)和长效β2受体激动剂福莫特罗(Formoterol)。
2022年11月10日,Viatris和Kindeva Drug Delivery赢得了一项重要的法院判决,美国西弗吉尼亚州北区地方法院裁定阿斯利康的Symbicort®专利,即美国专利号10166247无效。2023年7月,Viatris和Kindeva Drug Delivery宣布上市Breyna™(布地奈德和富马酸福莫特罗二水合物)吸入气雾剂,这是阿斯利康的 Symbicort® 获得美国食品药品监督管理局 (FDA) 批准的首个仿制药简化新药申请 (ANDA)。Breyna™ 的适应症包括 6 岁及以上患者的哮喘治疗,以及慢性阻塞性肺病(包括慢性支气管炎和/或肺气肿)患者的气流阻塞维持治疗和减少病情恶化。
7、Entresto(sacubitril/valsartan,诺欣妥):

Entresto由诺华开发,自2015年获批以来,一直是心力衰竭领域的主要药物。Entresto 2023年销售额为60.35亿美元,该药专利将于2024年5月到期。

图片来源:诺华财报
Entresto是sacubitril(一种脑啡肽酶[neprilysin]抑制剂)和缬沙坦(一种血管紧张素II受体阻断剂)组合复方,适用于在有慢性心力衰竭(NYHA类别II-IV)患者中减低对心力衰竭心血管死亡和住院的风险和减少射血分数。
Entresto最早于2015年7月获得美国FDA批准上市,是全球首款心衰治疗领域的突破性创新药物,并于2017年7月首次获批进入中国市场,2019年通过谈判纳入全国医保乙类目录,2021年成功续签,并新增原发性高血压适应症。
江苏华瀚医药取得了诺华在中国两项专利的完整许可,因此华瀚医药所开发的4类仿制药沙库巴曲缬沙坦钠片(商标名:悦欣妥®)可于专利保护期内在中国大陆市场合法上市销售(2024年3月15日起)。面对这块大蛋糕,国内外仿制药企早已虎视眈眈,Entresto面临着激烈的仿制药专利挑战,其中不乏中国药企(信立泰、石药欧意、正大天晴)。
8、Latuda(lurasidone HCl,盐酸鲁拉西酮):

Latuda由Sunovion Pharmaceuticals生产,是抗精神病药领域的关键产品之一。该药物被用于治疗精神分裂症,2022年销售额约为18亿美元。自2010年获批以来,Latuda已成为重要的治疗选择和太阳制药的主要收入来源。该药物部分专利将于2024年2月到期。
Latuda为5-HT及DA受体拮抗剂,此前已获FDA批准用于治疗成人精神分裂症,以及单药或与锂盐/丙戊酸联用治疗成人双相抑郁。

9、Xifaxan(Rifaximin,利福昔明):

胃肠道疾病是全球的主要治疗领域,肠易激综合征(IBS)是该领域的主要增长点。Salix Pharmaceuticals开发的Xifaxan 550 mg片剂是一种口服抗生素,适用于治疗成人腹泻性肠易激综合征(IBS-D)和降低成人明显肝性脑病(HE)复发的风险。
Xifaxan 2023年销售额18.1亿美元,该药部分专利将于2024年6月到期。
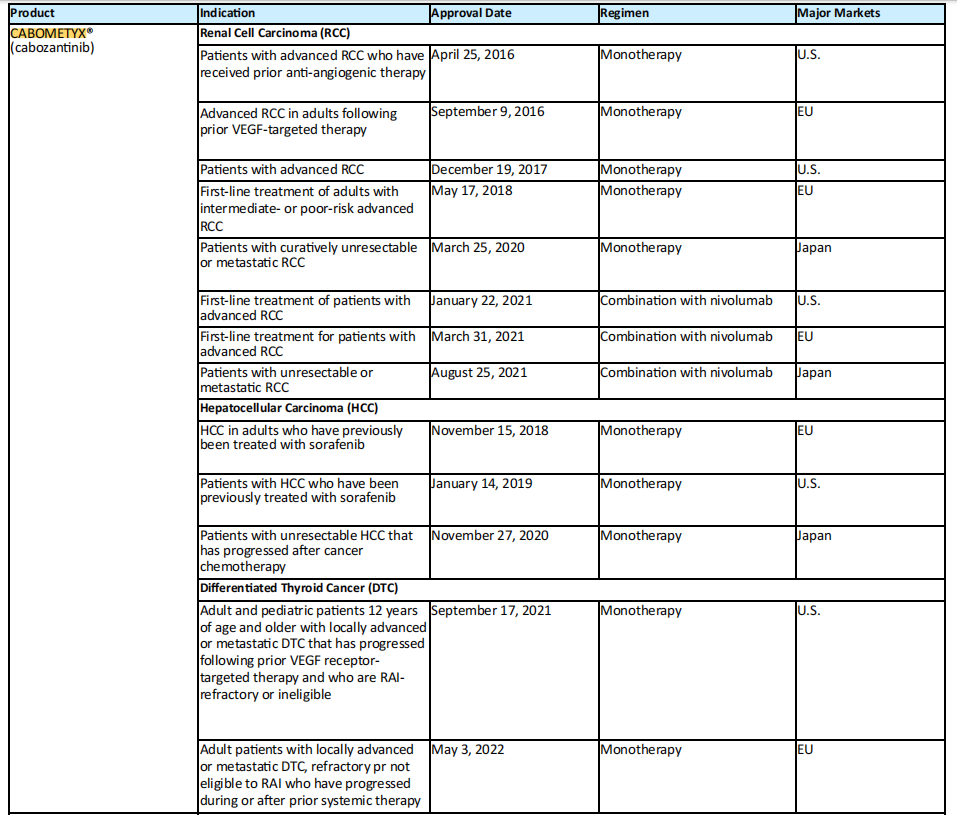
10、Cabometyx(Cabozantinib):

Cabometyx是Exelixis公司的一款重磅药物,2023年的销售额达到了约16.29亿美元。该药被批准用于治疗晚期肾细胞癌,既可作为一线治疗药物,也可在接受抗血管生成治疗后使用,该药部分专利将于2024年9月到期。
2016年4月,Cabometyx成为美国第一个批准用于既往治疗过的晚期肾细胞癌的单药疗法,在一项全球关键性试验中证明了三个关键疗效参数的统计学显著性和临床意义的改善:总生存期(OS)、无进展生存期(PFS)和客观缓解率(ORR)。到目前为止,Cabometyx仍然是唯一的单药疗法。
图片来源:Exelixis财报
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!













收藏
登录后参与评论